Publicado:
2015-03-19Número:
Vol. 11 Núm. 1 (2014)Sección:
Artículos de InvestigaciónDesarrollo de una técnica bioquímica para la degradación del espumado de poliuretano presente en colchones comercializados en Bogotá
Development of a biochemical technique for the degradation of polyurethane foamed used in mattress marketed in Bogotá
Descargas
Referencias
Alfaro, D., García, D., y Rodríguez J. “Obtención y caracterización de dos polímeros biodegradables con almidón de arroz en combinación con alcohol polivínilico o ácido acrílico”, Tesis de Pregrado Licenciatura en Química, Universidad Distrital Francisco José de Caldas, (2004).
Loza, H., y Cruz, J. en “Descubren en la UNAM bacteria que degrada el poliuretano” Boletín 007. Universidad Autónoma de México Facultad de Química, (2008).
Hincapié, G., y Ramírez, M. en “Biodegradación de Poliuretano Residual Aspergillus Níger” p. 1-12. Revista Investigaciones Aplicadas, Facultad de Ingeniería Agroindustrial, Universidad Pontificia Bolivariana, Medellín Antioquía (2008).
Troev, K., Grancharov, G., y Tsevi, R. en “A novel approach to recycling of polyurethanes: Chemical degradation of flexible polyurethane foams by triethyl phosphate” p. 7017-7022. Polymer Degradation and Stability, Institute of Polymers, Bulgarian Academy of Sciences, (2008).
“Norma Técnica Colombiana NTC 2019”, (Instituto Colombiano de Normas Técnicas y Certificación, ICONTEC), Primera actualización § (2008).
“Caracterización de aguas residuales por DBO y DQO”, Ingeniería de Tratamiento de Aguas Residuales p. 2-1 – 2-7 (2013).
Valdez, E., y Vázquez A. en “Ingeniería de los sistemas de tratamiento y disposición de aguas residuales” p. 30-32. Facultad de Ingeniería de la Universidad Nacional Autónoma de México, (2003).
Bermúdez, E., “Pruebas bioquímicas para evidenciar el crecimiento de bacterias” p. 1-30. Scribd World’s Digital library (2009).
Cómo citar
APA
ACM
ACS
ABNT
Chicago
Harvard
IEEE
MLA
Turabian
Vancouver
Descargar cita
Visitas
Descargas
Desarrollo de una técnica bioquímica para la degradación del espumado de poliuretano presente en colchones comercializados en Bogotá
Development of a biochemical technique for the degradation of polyurethane foamed used in mattress marketed in Bogotá
Adriana Milena Bonilla Bonilla & Néstor Alexánder Zambrano González1*, Josué Anselmo García Ortiz & Luis Francisco Becerra Galindo2
1.Estudiantes del Proyecto Curricular de Licenciatura en Química de la Universidad Distrital Francisco José de Caldas. milib05_28@hotmail.com; alexander1260@yahoo.com.mx
2. Director y codirector del trabajo de grado. Profesores de los programas de Licenciatura en Química y Licenciatura en Biología, respectivamente, de la Universidad Distrital Francisco José de Caldas.
Fecha de recepción: 15 de mayo de 2014
Fecha de aprobación: 15 de julio de 2014
Resumen
Se integraron dos técnicas que nunca antes habían sido utilizadas en el tratamiento de residuos sólidos de poliuretano provenientes de colchones. Una de las técnicas, de naturaleza biológica, fundamentada en la acción de la especie Aspergillus niger, conforme lo reportan investigadores de la Pontificia Universidad Bolivariana de Antioquia. La otra, de naturaleza química, propuesta por la Academia de Ciencias de Bulgaria, en la cual se utilizó fosfato de trietilo (FT) como agente químico que propicia la degradación del espumado de poliuretano.
La combinación de las técnicas, con una pequeña modificación y la inclusión de los agentes químicos y biológicos antes mencionados (Aspergillus niger y fosfato de trietilo), permitió desarrollar una nueva técnica bioquímica que incluyó la degradación (a pequeña escala) de dos muestras de espumado de poliuretano, luego de su utilización en la producción de colchones.
Palabras clave: espumado de poliuretano, degradación química, degradación biológica, demanda biológica de oxígeno (DBO).
Abstract
In this research we integrated two techniques which were used individually to polyurethane's solid waste treatment (those did not specifically use for manufacturing polyurethane mattress). One of them has a biological nature and it is based in the action's principles of Aspergillus niger species, according to Pontifical Bolivarian University of Antioquia researchers. And other technique has chemical nature. It was proposed by Academy of Sciences of Bulgaria, in which the triethyl phosphate (FT) was used like chemical to degradation polyurethane foaming.
Joining techniques allowed developing a new biochemical technique where degradation was achieved (small scale) about two polyurethane foam samples, then it was used in mattresses' production, thus for this purpose the combination and a slight variation in each one of the individual procedures which included the use of chemical and biological agents above (Aspergillus niger and triethyl phosphate).
Keywords: foamed polyurethane, chemical degradation, biological degradation, biological oxygen demand (BOD).
Introducción
La espuma de poliuretano es un material plástico poroso formado por una agregación de burbujas, conocido también con el nombre coloquial de goma espuma. Se forma básicamente por una reacción química de condensación de dos bases hidroxílicas combinadas con diisocianatos. Dicha reacción libera dióxido de carbono, gas que va formando las burbujas (Alfaro et al., 2004). Los poliuretanos son polímeros de adición por pasos, que se sintetizan siguiendo el esquema general que se muestra a continuación:
En la tabla 1 se muestran algunos dioles y diisocianatos muy utilizados para la síntesis de poliuretanos.
Uno de los procesos de producción del espumado de poliuretano reúne un grupo de reacciones químicas, que en su conjunto atienden a una polimerización por crecimiento en etapas, conforme se presenta en la figura 2.
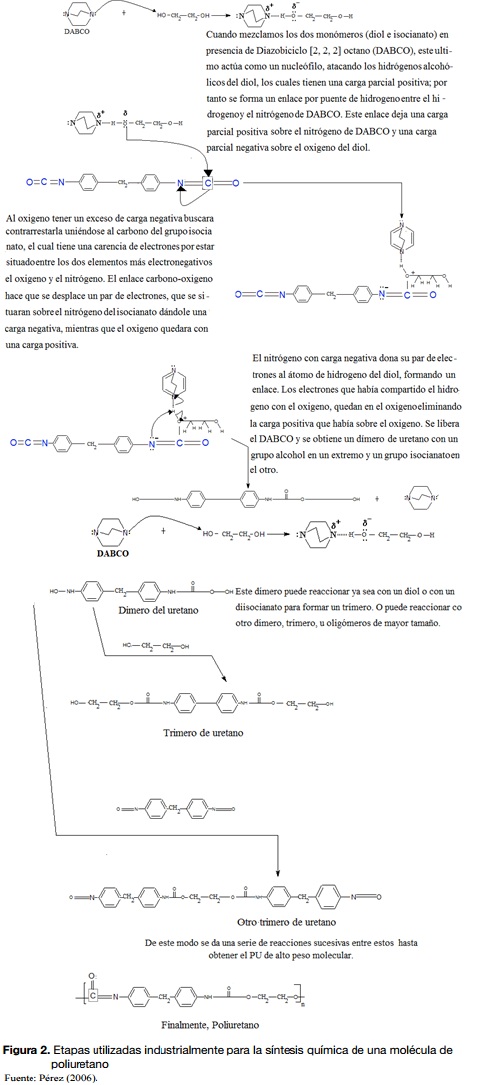
Dado que en la actualidad es muy fácil encontrarse con elementos construidos a base de poliuretano (pinturas, ruedas de patines y patinetas, partes elásticas de los tableros para vehículos, empaques para puertas y ventanas, espumas, rellenos de cojines y colchones, entre otros), resulta fundamental investigar acerca de la disposición final de este material –en sí misma muy compleja–, dado que el costo de este es relativamente bajo, su nivel de uso es extremadamente alto y su degradación natural, además de tardar varios años, genera subproductos de descomposición sumamente nocivos para la salud y el ambiente.
Estudios científicos como el de Loza y Cruz (2008) señalan: “Si bien es cierto que el poliuretano ha sido un desarrollo importante para la humanidad, cierto es también que es un problema desecharlo, porque no hay manera de destruirlo”.
Atendiendo a esta premisa, la comunidad científica ha desarrollado diferentes metodologías para alcanzar una degradación eficiente de este tipo de material; para ello ha utilizado procedimientos biológicos (Hincapié y Ramírez, 2008) y químicos (Troev et al., 2008) de manera independiente.
Para esta investigación se integraron dos técnicas: una de naturaleza biológica fundamentada en la acción de la especie Aspergillus niger, conforme lo reportan investigadores de la Pontificia Universidad Bolivariana de Antioquia (Hincapié y Ramírez, 2008), y otra de naturaleza química, propuesta por la Academia de Ciencias de Bulgaria, en la cual se utilizó fosfato de trietilo (FT) como agente químico que propicia la degradación del espumado de poliuretano (Troev et al., 2008).
La unión de ambas técnicas permitió desarrollar una nueva técnica bioquímica, con la cual se alcanzó la degradación (a pequeña escala) de dos muestras de espumado de poliuretano luego de ser utilizado en la producción de colchones; para tal fin se recurrió a la combinación de los procedimientos, es decir, se usaron los agentes químicos y biológicos mencionados.
Para el desarrollo de la etapa experimental se utilizaron dos muestras de espuma de poliuretano, clasificadas, de acuerdo con la norma técnica colombiana (NTC) 2019 (Icontec, 2008), en las clases 15 y 30, respectivamente.
En cuanto a la metodología, la investigación se dividió en dos fases: en la primera se sometió el espumado de poliuretano al ataque con el agente químico fosfato de trietilo (FT) –previamente caracterizado mediante IR– y en la segunda se alcanzó la adaptación del hongo Aspergillus niger en el espumado tratado químicamente, con la intención de remplazar su medio natural de alimentación, por poliuretano.
Metodología
Materiales y reactivos
Espuma de poliuretano proveniente de colchones comercializados en la ciudad de Bogotá, fosfato de trietilo (FT), Aspergillus niger, medio de cultivo para hongos B8, medio líquido basal enriquecido con glucosa e indicadores de pH (azul de lactofenol, rojo de metilo y azul de bromotimol).
Equipamiento
Equipo de reflujo, espectrofotómetro infrarrojo por transformada de Fourier de reflectancia total atenuada, respirómetro (Oxitop), incubadora, cámara de flujo laminar, potenciómetro, autoclave y microscopio digital.
Técnicas experimentales
Espectroscopía infrarroja por transformada de Fourier de reflectancia total atenuada (FT-IR – ATR), microscopía electrónica, respirometría, análisis cualitativos de variaciones de pH mediante el uso de indicadores, degradación química y degradación biológica.
Degradación química
Se cortaron 20 g de espumado de poliuretano en trozos de 3 a 5 mm de longitud y se adicionaron 60,21 ml del reactivo químico fosfato de trietilo (FT) en un matraz de tres bocas. A continuación se sometió la mezcla a reflujo, durante tres horas, a una temperatura de 190 °C. Finalmente se filtró el residuo y se ajustó el pH a 7,0 con solución de hidróxido de potasio (KOH) de concentración entre 0,5 y 1,5 M.
Degradación biológica
Se aisló el hongo filamentoso Aspergillus niger de una muestra de papa (Solanum tuberosum) en descomposición. La replicación de la cepa se llevó a cabo utilizando el medio basal enriquecido con glucosa. Luego de sembrar la cepa en tubos de ensayo mediante la técnica de estría, se procedió a la incubación por espacio de 120 horas.
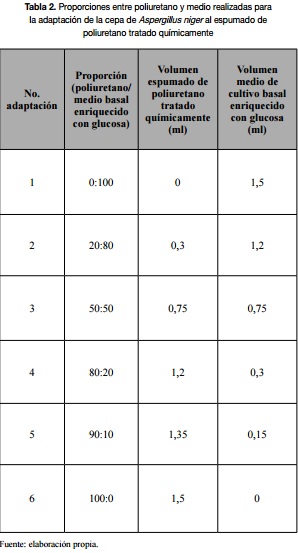
El hongo replicado se caracterizó microscópicamente y se dio inicio a los procesos de adaptación al espumado de poliuretano, previamente tratado en las proporciones sugeridas en la tabla 2. Posteriormente se aplicaron los ensayos de respirometría y las pruebas bioquímicas de variación de pH mediante indicadores, con el ánimo de estimar cualitativamente los resultados obtenidos.
Método de análisis de datos
Se utilizó la linealización, método gráfico de Thomas (Irustra y Fernández, 1999).
Resultados y discusión
Se realizó el análisis de las propiedades físicas, químicas y espectroscópicas de dos muestras de poliuretano utilizadas para la fabricación de colchones comercializados por una reconocida empresa, en Bogotá D. C., Colombia. La tabla 3 muestra los resultados de los análisis practicados a las muestras.
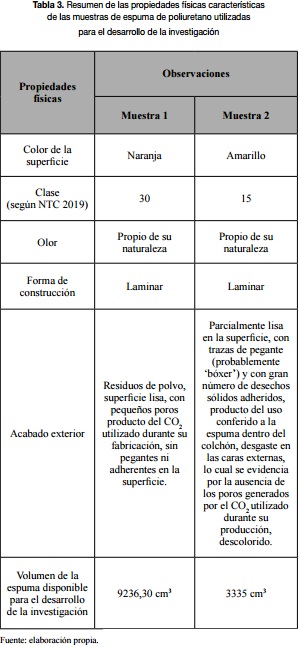
Con el ánimo de referenciar las muestras, en adelante se utilizarán las denominaciones muestra 1 y muestra 2, respectivamente. La muestra 1 corresponde al espumado de poliuretano con color de superficie naranja y clase 30, de acuerdo con lo establecido en la NTC 2019. La muestra 2 corresponde al espumado de poliuretano con color de superficie amarillo, clase 15, de acuerdo con lo establecido en la norma citada.
Para analizar las propiedades físicas y las características químicas del espumado de poliuretano utilizado se aplicaron algunos de los procedimientos sugeridos por el Icontec en la NTC 2019 (color de superficie, clase, acabado exterior, volumen, densidad y resistencia permanente a los solventes).
En relación con las propiedades espectroscópicas, se realizaron análisis de FT-IR – ATR a cada una de las muestras, antes y después del tratamiento, con el agente químico fosfato de trietilo (FT). Los espectros para la muestra 1, antes y después del tratamiento con el agente químico, se presentan en la figura 3.
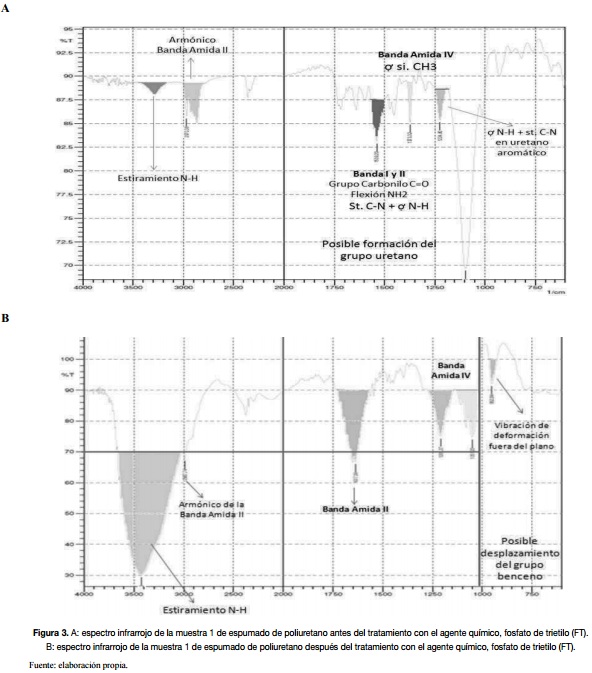
En cuanto a los espectros de las muestras antes del tratamiento con el agente químico se observó que en el aspecto estructural no se presentan diferencias importantes asociadas a sus elementos constitutivos (retardantes de llama, colorantes, entre otros), toda vez que se identificaron las bandas características del espumado de poliuretano: bandas N-H en una longitud de onda de 3300 cm-1 aproximadamente con replicaciones vibracionales simétricas y asimétricas entre 1533 cm-1 y 1373 cm-1, banda típica de los carbonilos de los grupos uretanos cerca de 1750 cm-1, y banda amida II, vibración asimétrica N-H que se ubica en 1539 cm-1 (banda de referencia en los estudios de Irustra y Fernández,1999)).
Los espectros realizados a las muestras sometidas a la degradación química, con posterior decantación, filtración y neutralización del producto obtenido, mostraron un aumento en la longitud de las bandas N-H, con leve desplazamiento e incremento de la transmitancia en las bandas amida II. Estos resultados coinciden con los estudios de Hincapié y Ramírez (2008), que indican la ruptura de las uniones que involucran al grupo uretano de la molécula de poliuretano y la liberación del grupo benceno presente.
Con referencia a la degradación química de cada una de las muestras, resulta importante precisar que se utilizaron algunos de los lineamientos del procedimiento propuesto por Troev et al. (2008), el cual utiliza montajes de reflujo para favorecer la reacción, tal como se presenta en la figura 4. Como producto del reflujo se obtuvo un líquido oscuro, viscoso y de una sola fase, situación que, conforme con los estudios de Troev et al. (2008), aporta algunos elementos conceptuales iniciales para clasificar el polímero en la subclase poliéster.
Tal como se señaló, el hongo Aspergillus niger se aisló de una papa (Solanum tuberosum) infectada en descomposición.
La parte infectada se inoculó en el medio líquido B8 y se replicó tres veces; se incubó cada muestra por una semana (en adelante la cepa producto de la aplicación de este procedimiento será nombrada Aislada_lab). Como factor de comparación se utilizó una cepa de Aspergillus niger 100 % caracterizada, proveniente del Servicio de Investigación Agrícola (ARS), agencia interna del Departamento de Agricultura de los Estados Unidos (USDA), cepa que en adelante, para efectos de referencia, se denominará USDA.
Una vez replicada la cepa aislada, fue observada a través de un microscopio digital con ayuda del indicador azul de lactofenol, lo cual permitió identificar claramente cada una de las partes constituyentes del hongo: célula o “pie”, conidióforos de pared lisa, vesículas globosas con conidios alrededor de ella y conidioesporas, conforme se presenta en la figura 5.
Teniendo en cuenta lo expuesto en el apartado metodológico del artículo (tabla 1), se realizaron las adaptaciones para ambas cepas de Aspergillus niger al espumado de poliuretano tratado químicamente. Se encontró que la adaptación número cinco fue la mejor de los seis casos implementados (proporción: 90 % poliuretano y 10 % medio).
Una vez alcanzada la mejor adaptación, se realizó una estimación semicuantitativa de la demanda biológica de oxígeno (DBO) a cinco días. Para implementar el ensayo se utilizó un equipo Oxitop BOX 15 WTW*. Los resultados se presentan en la tabla 4.
Dado que, teóricamente, durante los primeros días la tasa de disminución de oxígeno es rápida debido a la concentración grande de materia orgánica presente, al disminuir esta, también disminuye la tasa de consumo de oxígeno. Durante la última parte de la curva de la DBO el consumo de oxígeno se asocia con la decadencia de los organismos que crecieron durante la parte inicial de la prueba. Generalmente se supone que la tasa a la que se consume el oxígeno es directamente proporcional a la concentración de materia orgánica remanente en cualquier tiempo (Valdez y Vázquez, 2003).
Lo expuesto sugiere la importancia de hallar la DBO última (L), es decir, el máximo consumo de oxígeno posible cuando el desecho ha sido degradado por completo, así como la necesidad de calcular la constante de reacción (k). Con este propósito se tuvo en cuenta que matemáticamente la DBO puede ser descrita como una reacción de primer orden, en cuyo caso la constante de reacción (k) seguirá los parámetros definidos en la ecuación 1, y la DBO última (L), los parámetros presentados en la ecuación 2 (Valdez y Vázquez, 2003).
k fi = 6 B/A (ec. 1)
L fi = 1 / 6(A)2(B) (ec. 2)
Donde:
A: punto de intersección de la gráfica con el eje.
B: pendiente de la recta.
Posteriormente, para hallar el valor de la constante de reacción (k) y el valor de la DBO última (L), se recurrió al método gráfico de Thomas. Los resultados del método aplicado se presentan en la tabla 5.
De acuerdo con los resultados, se puede afirmar que el hongo Aspergillus niger es activo metabólicamente para biodegradar los residuos de poliuretano tratados previamente con el agente químico fosfato de trietilo (FT).
Los valores de la DBO última para esta investigación se alcanzaron en tiempos promedio que oscilan entre 5,34 y 6 días, lo que representa un avance importante para la degradación de este tipo de polímero al tomar como referente los hallazgos de los estudios de referencia de la Pontificia Universidad Bolivariana de Antioquia (Hincapié y Ramírez, 2008), en los cuales los valores de la DBO última se alcanzaron en un tiempo promedio de 8,3 días.
Finalmente, con el propósito de identificar cualitativamente el crecimiento del hongo en el espumado de poliuretano intervenido química y biológicamente, se aplicaron métodos de tinción con los indicadores rojo de metilo y azul de bromotimol, los cuales arrojaron resultados consistentes con la vía metabólica del Aspergillus ger [12], conforme se presenta brevemente a continuación.
Rojo de metilo
La prueba del indicador rojo de metilo es cualitativa para la producción de ácido y requiere de organismos positivos que produzcan ácidos láctico, acético o fórmico a partir de la glucosa, lo cual resulta apropiado para el estudio de la ruta metabólica de la especie Aspergillus niger, la cual produce, entre otros, ácido cítrico, ácido oxálico, glicerol y glucosa (Reyes et al., 2012).
Los resultados cualitativos encontrados en las cepas Aislada_lab y USDA, después de la aplicación de la prueba bioquímica con el indicador rojo de metilo, se presentan en la figura 6 y la tabla 6.
* En el análisis del resultado de esta prueba es importante recordar que, luego de la fase de degradación química, se realizó un proceso de neutralización con hidróxido de potasio, razón por la cual el pH de la muestra se ubicó alrededor de 7,0.
Debido a que los resultados cualitativos de esta prueba son positivos para ambas cepas, es posible afirmar que posterior a cinco (5) días de incubación, existe una producción significativa de ácido en la muestra, lo cual supone crecimiento del hongo, en el poliuretano químicamente tratado.
Azul de bromotimol
Esta prueba permite determinar si un organismo es capaz de metabolizar ácidos, lo cual generará una fuerte acidificación del medio, que será aparente por un cambio de color en el indicador de pH (Bermúdez, 2009).
Los resultados cualitativos encontrados en las cepas Aislada_lab y USDA, posteriores a la aplicación de la prueba bioquímica con el indicador azul de bromotimol, se presentan en la figura 7.
A partir de las estimaciones de referencia mostradas en la tabla 7, los resultados para esta prueba son positivos, toda vez que se produce una coloración amarilla en los tubos de ensayo, la cual se mantiene invariable a lo largo del tiempo (evidencia de acidificación del medio).
Conclusiones
De acuerdo con los resultados, se concluye que la técnica bioquímica propuesta en esta investigación para la degradación del espumado de poliuretano presente en colchones comercializados en Bogotá resulta apropiada para el tratamiento (a pequeña escala) de dicho material polimérico.
En comparación con técnicas de degradación de naturaleza estrictamente biológica, el tratamiento previo del espumado de poliuretano con agentes químicos, como el fosfato de trietilo (FT), resulta fundamental para el mejoramiento de los niveles de adaptación que alcanza el hongo al entrar en contacto con el material polimérico.
La relación 90 % de espumado de poliuretano: 10 % medio fue la mejor adaptación alcanzada.
El medio líquido basal, enriquecido con glucosa, resultó fundamental para proporcionar al hongo los nutrientes básicos que, junto con el carbono y el nitrógeno proporcionado por el poliuretano y el exceso de fósforo aportado por el fosfato de trietilo, permitieron la supervivencia y el desarrollo dentro de la muestra.
El ensayo respirométrico permitió la estimación del consumo completo del oxígeno presente en el Oxitop aproximadamente a los 6 días (144 horas). Este resultado indica que en ese tiempo el microorganismo estuvo listo para iniciar una biodegradación de tipo primario. Otros estudios han reportado resultados similares al cabo de 200 horas.
Espectroscópicamente, se corroboraron algunas hipótesis que apuntan hacia la ruptura del entrecruzamiento existente entre las cadenas del polímero, a causa de la acción del agente químico fosfato de trietilo (aumento de transmitancia en las bandas amida II y IV (ruptura enlaces N-H y C-N) y liberación de anillos aromáticos). Así mismo, se observó que la estructura básica del polímero sin tratar no presentaba interferencias importantes asociadas a sus elementos constitutivos (retardantes de llama, colorantes, entre otros).
Finalmente, en relación con los resultados de los ensayos realizados con los indicadores de pH, se puede afirmar que existe una alta tendencia de la muestra a la acidificación, producto de la vía metabólica del microorganismo seleccionado para la implementación de la degradación biológica.
Referencias
Alfaro, D., García, D. y Rodríguez J. (2004). Obtención y caracterización de dos polímeros biodegradables con almidón de arroz en combinación con alcohol polivinílico o ácido acrílico. Tesis de pregrado, Licenciatura en Química, Universidad Distrital Francisco José de Caldas.
Bermúdez, E. (2009). Pruebas bioquímicas para evidenciar el crecimiento de bacterias. Scribd World’s Digital Library.
Gregory, B., Alba, L., Brown, A., Fernández, M., Moura, J., De la Hoz, Y. y Álvarez, A. (2007). Los poliuretanos biodegradables: estudio bibliográfico de su síntesis y aplicaciones. La Habana: Instituto Cubano de Investigaciones de los Derivados de la Caña de Azúcar.
Hincapié, G. y Ramírez, M. (2008). Biodegradación de poliuretano residual Aspergillus niger. En Investigaciones Aplicadas, Facultad de Ingeniería Agroindustrial, Universidad Pontificia Bolivariana, Medellín.
Icontec. (2008). Norma técnica colombiana NTC 2019, primera actualización.
Irustra, L. y Fernández, B. (1999). Aplicación de la espectroscopía infrarroja transformada de Fourier al estudio de recubrimientos de poliuretano. Revista de Plásticos Modernos, 78, 245-254.
Loza, H. y Cruz, J. (2008). Descubren en la UNAM bacteria que degrada el poliuretano. Boletín No. 007, Universidad Autónoma de México, Facultad de Química.
Pérez, J. (2006). Historia del poliuretano: orígenes y actualidad. Química y Tecnología de Macromoléculas, Escuela de Ingenierías Industriales Uva. Recuperado de http://www.eis.uva.es/~macromol/curso05-06/pu/historia.htm.
Reyes Ocampo, I., González-Brambila M. y López-Isunza, F. (2012). Un análisis del metabolismo de Aspergillus niger creciendo sobre un sustrato sólido. Revista Mexicana de Ingeniería Química, 12 (1), 41-43.
Troev, K., Grancharov, G. y Tsevi, R. (2008). A novel approach to recycling of polyurethanes: Chemical degradation of flexible polyurethane foams by triethyl phosphate. In Polymer Degradation and Stability. Institute of Polymers, Bulgarian Academy of Sciences.
Valdez, E. y Vázquez A. (2003). Ingeniería de los sistemas de tratamiento y disposición de aguas residuales. Facultad de Ingeniería de la Universidad Nacional Autónoma de México.
Agradecimientos
Al Laboratorio de Servicios Públicos, Facultad de Medio Ambiente y Recursos Naturales, Universidad Distrital Francisco José de Caldas.
A la Vicerrectoría de Investigación, Innovación, Creación, Extensión y Proyección Social, de la Universidad Distrital Francisco José de Caldas, por la financiación de la investigación.
Licencia
Tecnogestión esta bajo una licencia Creative Commons - 4.0 Colombia License.
Atribución - No Comercial - Sin Derivadas




