DOI:
https://doi.org/10.14483/2256201X.23642Publicado:
01-01-2026Número:
Vol. 29 Núm. 1 (2026): Enero-junioSección:
Artículos de investigación científica y tecnológicaViabilidad y capacidad germinativa en semillas de Pterocaulon alopecuroides (Lam.) DC., una planta de uso medicinal
Viability and Germination Capacity in Seeds of Pterocaulon alopecuroides (Lam.) DC., a Plant for Medicinal Use
Palabras clave:
Cypsela, germination, latency, dormancy (en).Palabras clave:
cipsela, germinación, latencia, dormancia (es).Descargas
Referencias
Adegbola, Y. U., & Pérez, H. E. (2016). La extensa desecación y la tolerancia al estrés por envejecimiento caracterizan las semillas de Gaillardia pulchella (Asteraceae). HortScience, 51(2), 159-163. https://doi.org/10.21273/HORTSCI.51.2.159
Azcón-Bieto, J., & Talón, M. (2000). Fundamentos de fisiología vegetal. Editorial McGraw-Hill Interamericana.
Bakker, J. (2001). Seeds, ecology, biogeography and evolution of dormancy, and germination. C. C. Baskin & J. M. Baskin. Plant Ecology, 152, 204-205. https://doi.org/10.1023/A:1011465920842
Baskin, C. C., & Baskin, J. M. (2023). Seed dormancy in Asteraceae: A global vegetation zone and taxonomic/phylogenetic assessment. Seed Science Research, 33(2), 135-169. https://doi.org/10.1017/S0960258523000107
Bewley, J. D. (1997). Seed germination and dormancy. The Plant Cell, 9(7), 1055-1066. https://doi.org/10.1105/tpc.9.7.1055
Bewley, J. D., Bradford, K., Hilhorst, H., & Nonogaki, H. (2013). Seeds: Physiology of development, germination and dormancy (3ra ed.). Editorial Springer.
Cabrera, Á. L., & Ragonese, A. M. (1978). Revisión del género Pterocaulon (Compositae). Darwiniana, 21(2/4), 185-257. http://www.jstor.org/stable/23215593
Caroca, R., Zapata, N., & Vargas, M. (2016). Efecto de la temperatura sobre la germinación de cuatro genotipos de maní (Arachis hypogaea l.). Chilean Journal of Agricultural & Animal Science, 32(2), 94-101. http://dx.doi.org/10.4067/S0719-38902016000200002
Cuatrecasas, J. (1958). Aspectos de la vegetación natural de Colombia. Academia Colombiana de Ciencias, Exactas, Físicas y Naturales, 41, 100-132. https://doi.org/10.18257/raccefyn.570
Doria, J. (2010). Generalidades sobre las semillas: su producción, conservación y almacenamiento. Cultivos Tropicales, 31(1), 74-85. http://scielo.sld.cu/pdf/ctr/v31n1/ctr11110.pdf
Funk, V. A., Susanna, A., Stuessy, T. F., & Bayer, R. J. (2009). Systematics, evolution, and biogeography of Compositae. Editorial International Association for Plant Taxonomy.
Godoi, S., & Takaki, M. (2004). Effects of light and temperature on seed germination in Cecropia hololeuca Miq. (Cecropiaceae). Brazilian Archives of Biology and Technology, 47(2), 185-191. https://doi.org/10.1590/S1516-89132004000200004
Gonzáles, M. A., & Quintero, L. (2017). Plantas: recolección y preservación. En M. A. González Y. & H. Arenas-Castro (Eds.), Recolección de tejidos biológicos para análisis genéticos (pp. 11-12). Editorial Espacio Creativo Impresores S. A. S.
González, M. P., Quiroz, I., García, E., & Gutiérrez, B. (2008). Escarificación química con ácido sulfúrico como tratamiento pregerminativo para semillas de Toromiro (Sophora toromiro Skottsb. Ciencia & Investigación Forestal, 14(1), 111-118. https://doi.org/10.52904/0718-4646.2008.95
González-Rodríguez, F., Borges-Gómez, L., Pinzón-López, L., Magaña-Magaña, M., Sanginés-García, R., & Urrestarazu-Gavilán, M. (2014). Immersion of maize seeds in hot water as a treatment to estimulate sprout production for forage. Agronomía Mesoamericana, 25(1), 53-62. https://doi.org/10.15517/am.v25i1.14197
Guo, C., Shen, Y., & Shi, F. (2020). Effect of temperature, light, and storage time on the seed germination of Pinus bungeana Zucc. ex Endl.: The role of seed-covering layers and abscisic acid changes. Forests, 11(3), 300. https://doi.org/10.3390/f11030300
Unión Internacional para la Conservación de la naturaleza (UICN) (2025, 8 de septiembre). The IUCN Red List of Threatened Species. https://www.iucnredlist.org
Illinki, V., Yankova-Tsvetkova, E., & Stanilova, M. (2020). Germination and viability of seeds of Tanacetum cinerariifolium (Asteraceae). Comptes rendus de l’Académie bulgare des Sciences, 73(7), 965-970. https://doi.org/10.7546/CRABS.2020.07.09
Instituto Geográfico Agustín Codazzi (IGAC) (2006). Métodos analíticos del laboratorio de suelos (6a ed.). Departamento Administrativo Nacional de Estadística.
Jackson, S. D. (2009). Plant responses to photoperiod. New Phytologist, 181(3), 517-531. https://doi.org/10.1111/j.1469-8137.2008.02681.x
Jiménez-Vázquez, A. M., Flores-Palacios, A., Flores-Morales, A., Perea-Arango, Irene., Gutiérrez, M. C., Arellano-García, J. J., & Valencia-Díaz, S. (2021). Seed longevity, viability and germination of four weed-ruderal Asteraceae species of ethnobotanic value. Botanical Sciences, 99(2), 279-290. https://doi.org/10.17129/botsci.2743
Kiewnick, L. (1964). The phytomelanin layer in the pericarp of Helianthus annuus as a barrier against Homoeosomane bulella. Zeitschrift für Pflanzenkrankheiten (Pflanzenpathologie) und Pflanzenschutz, 71, 294-301.
Makhaye, G., Mofokeng, M. M., Tesfay, S., Aremu, A. O., Van Staden, J., & Amoo, S. O. (2021). Influence of plant biostimulant application on seed germination. En S. Gupta & J. van Staden (Eds.), Biostimulants for Crops from Seed Germination to Plant Development (pp. 109-135). Elsevier. https://doi.org/10.1016/b978-0-12-823048-0.00014-9
Mancipe-Murillo, C., Calderón-Hernández, M., & Pérez-Martínez, L. V. (2018). Evaluación de viabilidad de semillas de 17 especies tropicales altoandinas por la prueba de germinación y la prueba de tetrazolio. Caldasia, 40(2), 366-382. https://doi.org/10.15446/caldasia.v40n2.68251
Marques, D., e Cândido, J. B., Loeuille, B., & Marzinek, J. (2022). Comparative morphology and anatomy of cypselae in Piptolepis (Vernonieae, Asteraceae) with emphasis on the pappus systematic significance. Flora, 287, 151988. https://doi.org/10.1016/j.flora.2021.151988
Mathur, R. R., Shekhar, S., & Pandey, A. K. (2024). Phytomelanin in Asteraceae: A review. The Journal of the Indian Botanical Society, 104(4), 210-221. https://doi.org/10.61289/jibs2024.06.05.265
Matsoukas, I. G. (2014). Attainment of reproductive competence, phase transition, and quantification of juvenility in mutant genetic screens. Frontiers in Plant Science, 5, 1-5. http://doi.org//0.3389/fpls.2014.00032
Mayer, A. M., & Poljakoff-Mayber, A. (2014). The germination of seeds. Elsevier.
Medeiros-Neves, B., Teixeira, H. F., & von Poser, G. L. (2018). The genus Pterocaulon (Asteraceae) – A review on traditional medicinal uses, chemical constituents and biological properties. Journal of Ethnopharmacology, 224, 451-464. https://doi.org/10.1016/j.jep.2018.06.012
Moreno, F., Plaza, G. A., & Magnitskiy, S. V. (2006). Efecto de la testa sobre la germinación de semillas de caucho (Hevea brasiliensis Muell.). Agronomía Colombiana, 24(2), 290-295. https://www.scielo.org.co/scielo.php?script=sci_arttext&pid=S0120-99652006000200011
Navarro García, G. (2013). Química agrícola: química del suelo y de los nutrientes esenciales para las plantas. Ediciones Mundi-Prensa.
Negbi, M., Black, M., & Bewley, D. (1968). Far-red sensitive dark processes essential for light- and gibberellin-induced germination of lettuce seed. Plant Physiology 43, 35-40. https://doi.org/10.1104/pp.43.1.35
Olander, S., & Tyler, T. (2017). Morphometrics and taxonomy of Erigeron acris sensu lato (Asteraceae) in Fennoscandia. New Journal of Botany, 7(1), 39-50. https://doi.org/10.1080/20423489.2017.1344076
González-M. R., Thomas, E., Vásquez, A., Pizano, C., Medina, A., González, A. F., Acosta Galvis, R. A., & García. (2016). El bosque seco tropical en Colombia. En M. F. Gómez, L. A Moreno, G. I. Andrade & C. Rueda (Eds.), Biodiversidad 2015. Estado y Tendencias de la Biodiversidad Continental de Colombia (pp. 108). Instituto Alexander von Humboldt.
Pizano, C., Cabrera, M., & García, H. (2014). Bosque seco tropical en Colombia; generalidades y contexto. Instituto de Investigación de Recursos Biológicos Alexander von Humboldt.
Pliszko, A., & Kostrakiewicz-Gierałt, K. (2020). Effect of pappus removal on seed germination in Solidago ×niederederi (Asteraceae) and closely related species. Biologia, 75, 1241-1249. https://doi.org/10.2478/s11756-020-00506-x
Polindara-Moncayo, Y. W., & Sanabria Diago, O. L. (2024). Plantas de la medicina tradicional en El Tambo, Cauca. Editorial Universidad del Cauca.
Polindara-Moncayo, Y. W., & Sanabria-Diago, O. L. (2022). Plants and conservation practices of traditional medicine in the southeast of El Tambo, Cauca, Colombia. Botanical Sciences, 100(4), 935-959. https://doi.org/10.17129/botsci.3056
Pompelli, M. F., Jarma-Orozco, A., & Rodriguez-Páez, L. A. (2023). Imbibition and germination of seeds with economic and ecological interest: Physical and biochemical factors involved. Sustainability, 15(6), 1-24. https://doi.org/10.3390/su15065394
Popay, A. I., & Roberts, E. H. (1970). Factors involved in the dormancy and germination of Capsella bursa- pastoris (L.) Medik. and Senecio vulgaris L. Journal of Ecology, 58(1), 103-122. https://doi.org/10.2307/2258171
Posit team (2025). RStudio: Integrated development environment for R. Posit Software, PBC. http://www.posit.co
R Core Team (2025). R. A language and environment for statistical computing. R Foundation for Statistical Computing. https://www.R-project.org
Reina-García, J.D., Almaguer-Vargas, G., Cruz-Castillo, J. G., Guerra-Ramírez, D., & Castañeda-Vildozola, Á. (2024). Sulfuric acid as a germination stimulator in forage soybean seeds (Neonotonia wightii). Revista Facultad Nacional de Agronomía Medellín, 77(3), 10833-10838. https://doi.org/10.15446/rfnam.v77n3.109179
Ren, Z., & Abbott, R. J. (1991). Seed dormancy in Mediterranean Senecio vulgaris. New Phytologist, 117(4), 673-678. https://doi.org/10.1111/j.1469-8137.1991.tb00972.x
Rodrigues de Queiroz, A., & Maricle, B. R. (2019). Effects of light levels on germination of five Asteraceae species native to the tallgrass prairie. Transactions of the Kansas Academy of Science 122(3/4), 267-273. http://www.jstor.org/stable/45221239
Roeber, V. M., Schmülling, T., & Cortleven, A. (2022). The photoperiod: Handling and causing stress in plants. Frontiers in Plant Science, 12, 1-14. https://doi.org/10.3389/fpls.2021.781988
Rolnik, A. & Olas, B. (2021). The plants of the Asteraceae Family as agents in the protection of human health. International Journal of Molecular Sciences, 22(6), 1-10. https://doi.org/10.3390/ijms22063009
Royal Botanic Gardens, Kew (s.f.). Pterocaulon virgatum (L.) DC. Plants of the World Online. https://powo.science.kew.org/taxon/urn:lsid:ipni.org:names:10743-1
Sanabria, D., Silva, R., Oliveros, M., & Barrios, R. (2001). Escarificación química y térmica de semillas subterráneas de Centrosema rotundifolium. Bioagro, 13(3), 117-124. https://www.redalyc.org/articulo.oa?id=85713305
Sanabria-Diago, O. L., Hernández-Bernal, E., & Polindara-Moncayo Y. W. (2022). Manual de etnobotánica para colectas en campo (pp. 21-29). Editorial Biblioteca Nacional de Colombia.
Sharma, S., Singh, V., Hemender Tanwar, Mor, V. S., Kumar, M., Punia, R. C., Dalal, M. S., Khan, M., Sangwan, S., Bhuker, A., Dagar, C. S., Yashveer, S., & Singh, J. (2022). Impact of high temperature on germination, seedling growth and enzymatic activity of wheat. Agriculture, 12(9), 1500. https://doi.org/10.3390/agriculture12091500
Szczerba, A., Płażek, A., Pastuszak, J., Kopeć, P., Hornyák, M., & Dubert, F. (2021). Effect of low temperature on germination, growth, and seed yield of four soybean (Glycine max L.) cultivars. Agronomy, 11(4), 800. https://doi.org/10.3390/agronomy11040800
Talská, R., Machalová J., Smýkal P., & Hron K. (2020). A comparison of seed germination coefficients using functionalregression. Applications in Plant Sciences, 8(8), 1-11. https://doi.org/10.1002/aps3.11366
Valdivia, F. & Espinoza, A. (2019). Evaluación visual de suelos (1ra ed., vol. 2). Catholic Relief Services.
Vandana, U. K., Singha, B., Gulzar, A., & Mazumder, P. (2020). Molecular mechanisms in plant growth promoting bacteria (PGPR) to resist environmental stress in plants. En V. Sharma, R. Salwan & L. K. Tawfeeq Al-ani (Eds.), Molecular Aspects of Plant Beneficial Microbes in Agriculture (pp. 221-233). Elsevier. https://doi.org/10.1016/b978-0-12-818469-1.00019-5
Zhang, T., & Elomaa, P. (2024). Development and evolution of the Asteraceae capitulum. New Phytologist, 242(1), 33-48. https://doi.org/10.1111/nph.19590
Cómo citar
APA
ACM
ACS
ABNT
Chicago
Harvard
IEEE
MLA
Turabian
Vancouver
Descargar cita
Recibido: 22 de mayo de 2025; Aceptado: 3 de octubre de 2025
Resumen
Pterocaulon alopecuroides es una especie de relevancia ecológica y cultural del municipio de El Tambo, Cauca, Colombia, por lo cual se evaluó su viabilidad con tetrazolio (TZ). Se tomaron medidas de la longitud-peso de las cipselas y la capacidad germinativa bajo los siguientes tratamientos: escarificación química (EQ), inmersión térmica (IT), evaluación térmica en ausencia de luz (ETAL), exposición a distintas longitudes de onda (EDLO), tipología de suelos (TS) y un fotograma de desarrollo germinativo. Los resultados obtenidos mostraron la viabilidad y capacidad germinativa de la especie, relacionada con el tamaño y peso de las semillas. Como respuesta a la EQ con H₂SO₄ al 20 % por dos minutos, se registró un 50 % de germinación, así como 30 % en suelos franco-arenosos, 10 % con luz roja-cercana en EDLO, 2 % con IT y 0 % en la ETAL. Esta investigación proporciona una base científica para generar estrategias de conservación y propagación de P. alopecuroides en contextos bioculturales.
Palabras clave:
cipsela, germinación, latencia, dormancia.Abstract
Pterocaulon alopecuroides is a species of ecological and cultural significance in the municipality of El Tambo, Cauca, Colombia, which is why we evaluated its viability using tetrazolium (TZ). We measured the length and weight of the cypselae and the germination capacity under the following treatments: chemical scarification (CS), thermal immersion (TI), thermal evaluation in the absence of light (TEAL), exposure to different wavelengths (EDW), soil typology (ST), and a germination development photogram. The results indicated the viability and germination capacity of the species, which are related to seed size and weight. In response to CS with 20% H₂SO₄ for two minutes, a 50% germination rate was recorded, as well as 30% in loamy-sandy soils, 10% under near-red light in EDW, 2% with TI, and 0% in the TEAL. This research provides a scientific basis for developing conservation and propagation strategies for P. alopecuroides in biocultural contexts.
Keywords:
cypsela, germination, latency, dormancy.INTRODUCCIÓN
El origen de la familia Asteraceae se remonta al cretácico superior, hace 83 millones de años en Sudamérica, donde se dispersó hacia África y Asia. Actualmente, esta familia comprende 1600 géneros y alrededor de 30 000 especies (Zhang & Elomaa, 2024). Dentro de ella está el género Pterocaulon, conformado por 26 especies, de las cuales 12 se distribuyen en sistemas socioecológicos que van desde el sur de los Estados Unidos hasta el centro de Argentina. Entre estas especies se encuentran P. alopecuroides, P. angustifolium, P. balansae, P. cordobense, P. lanatum, P. lorentzii, P. polypterum, P. polystachyum, P. purpurascens, P. pycnostachyum, P. rugosum y P. virgatum (Cabrera & Ragonese, 1978; Rolnik & Olas, 2021).
De las 12 especies reportadas, únicamente P. virgatum y P. alopecuroides se encuentran presentes en Colombia, y su rango altitudinal de distribución oscila entre los 280 y los 2630 m (Royal Botanic Garden, Kew, s.f.). Esta última, tradicionalmente conocida como árnica de loma se caracteriza por ser una hierba perenne con tallos alados, tomentosos, hojosos y erectos, que alcanza una longitud entre 70 y 150 cm. Presenta un xilopodio globoso, del cual nacen raíces delgadas y tallos encargados de almacenar agua y nutrientes en épocas de sequía. Sus inflorescencias están conformadas por capítulos pequeños dispuestos en espigas, glomérulos y/o panojas, con flores masculinas y femeninas. Los frutos son tipo cipsela, caracterizados por ser velludos, con glándulas esféricas sésiles y por tener costillas conspicuas. El papus es de color blanco, biseriado con secuencias internas y externas de tamaño similar a los de Piptolepis ericoides, una estructura que ha sido considerada como un carácter exitoso en la dispersión del género Pterocaulon (Cabrera & Ragonese, 1978; Marques et al., 2022).
Por ende, como unidad de germinación, la cipsela constituye una estructura resistente a la desecación, lo que ha facilitado la diversificación, al igual que el xilopodio. En este contexto, las semillas de la familia Asteraceae juegan un papel fundamental en el ciclo de vida de las plantas, pues su desarrollo está influenciado por factores como el sustrato (tipología de suelos), el agua, el aire (anemofilia y anemocoria), la altitud, la temperatura (bajas: 10-15 °C; altas 20-25 °C), el fotoperiodo y la presencia de pigmentos como la fitomelanina (Talská et al., 2020; Mathur et al. 2024). Estos elementos llevan a la elongación del eje embrionario de las semillas, que comprende tres fases: (i) imbibición de la semilla, (ii) reactivación del metabolismo y (iii) aparición de la radícula (Makhaye et al., 2021; Pompelli et al., 2023).
P. alopecuroides ha sido utilizada y propagada a través de sus semillas por los sistemas médicos tradicionales, que vinculan formas de manejo (colecta y siembra), preparación y administración a través de las parteras, los médicos ancestrales, los sobanderos y los yerbateros de comunidades afrodescendientes, campesinas e indígenas, quienes tratan enfermedades de la piel, heridas y dolencias hepáticas con partes de la planta (semillas, hojas, tallos y raíces, o su totalidad). Esta planta ha resultado efectiva debido a sus propiedades antifúngicas, antivirales, citotóxicas y antioxidantes, que contribuyen al bienestar de la salud humana y a la conservación de las prácticas bioculturales presentes en El Tambo (Polindara-Moncayo & Sanabria, 2022). Por ello, esta especie promisoria y de relevancia etnobotánica requiere estudios que busquen conocer su viabilidad y capacidad germinativa bajo condiciones y tratamientos distintos, puesto que hay vacíos en la literatura científica sobre sus protocolos de propagación y conservación (UICN, 2025).
P. alopecuroides es una especie medicinal con un amplio rango de distribución que va desde ecosistemas como el bosque seco tropical hasta la selva subandina. No obstante, su hábitat se encuentra amenazado por factores como la extracción directa y masiva, incendios recurrentes, expansión de la frontera agrícola de monocultivos, ganadería extensiva y la minería a cielo abierto (Cuatrecasas, 1958; Pizano et al., 2014; Pizano et al., 2016). En este contexto, resulta prioritario establecer metodologías fisicoquímicas para evaluar la capacidad y viabilidad germinativa de semillas nativas de esta especie medicinal con base en tratamientos como la escarificación química (EQ), la inmersión térmica (IT), la evaluación térmica en ausencia de luz (ETAL), la exposición a distintas longitudes de onda (EDLO) y la tipología de suelos (TS) (Vandana et al., 2020).
MATERIALES Y MÉTODOS
Zona de estudio
El municipio de El Tambo (Cauca, Colombia) comprende un área de 3280 km² y se encuentra ubicado entre las regiones biogeográficas del Pacífico y los Andes colombianos (Polindara & Sanabria, 2022). En este territorio se localiza la vereda Los Llanos (02°47'11.5'' N, 76°76'06.65'' O), a una altitud de 1652 m, correspondiente al ecosistema de selva subandina (Cuatrecasas, 1958). De esta zona se recolectaron 1474 semillas de P. alopecuroides entre agosto de 2023 y abril de 2024 (época de sequía) para realizar las respectivas pruebas de viabilidad y capacidad germinativa.
Herborización y colecta de semillas
En colaboración con la comunidad campesina de la vereda Los Llanos, se realizaron recorridos en áreas de potreros y rastrojos, identificados como hábitat potencial de la especie. De aquí se recolectaron cuatro muestras en estado fértil, las cuales fueron embebidas en etanol al 70 %, deshidratadas, montadas, identificadas e incluidas en la colección general del herbario CAUP (052 658) de la Universidad del Cauca. Paralelamente, se seleccionaron y recolectaron 1474 semillas de P. alopecuroides con tonalidad marrón-oscura entre agosto de 2023 y abril de 2024 para realizar las pruebas mencionadas. Este material fue almacenado en bolsas de papel y, posteriormente, en bolsas plásticas de cierre hermético, de conformidad con el Manual de etnobotánica para colectas en campo y el documento titulado Recolección de tejidos biológicos para análisis genéticos (González & Quintero, 2017; Sanabria et al., 2022).
Medición y peso de las semillas
Tras el proceso de herborización, se seleccionó una muestra aleatoria de 20 semillas, con el objetivo de realizar mediciones morfométricas centradas en el peso, longitud de la cipsela y el papus. La metodología empleada se fundamentó en los lineamientos propuestos por Olander y Tyler (2017).
Viabilidad y capacidad germinativa
Viabilidad
La viabilidad se evaluó agregando 10 mL de tetrazolio (TZ) o cloruro de 2,3,5-trifeniltetrazolio al 1 % sobre papel filtro al interior de una caja Petri, no expuesta a la luz y a temperatura ambiente (23 °C) durante 1 h, en la cual se colocaron 20 cipselas cortadas longitudinalmente, procurando que la superficie de la semilla y el embrión quedaran en contacto con la solución (Jiménez-Vázquez et al., 2021). Transcurrido este tiempo, se procedió a contabilizar los embriones coloreados con rojo (viables) y los incoloros (inviables). Posteriormente, se calculó el porcentaje de viabilidad con base en lo planteado por Azcón-Bieto y Talón (2000).
Prueba de imbibición
Siguiendo la metodología descrita por Moreno et al. (2006), se prepararon tres lotes de 50 cipselas, los cuales fueron hidratados a través de inmersión en 3, 5 y 7 mL de H2O destilada por 30 min. Finalizado el proceso de hidratación, las semillas fueron secadas con papel absorbente y pesadas en una balanza analítica (AS 220.R2 PLUS, RADWAG Balances & Scales). La masa de cada muestra fue registrada cada media hora hasta alcanzar la estabilización del peso. Este procedimiento fue replicado diez veces.
Capacidad germinativa
Se evaluó la emergencia de la radícula bajo condiciones de laboratorio y distintos tratamientos pre-germinativos (EQ, IT, ETAL, EDLO y TS). Con base en los resultados obtenidos en los ensayos, se estimó el porcentaje de germinación mediante la siguiente ecuación.
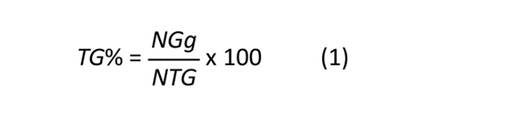
Donde:
-
TG %: porcentaje de germinación
-
NGg: número de semillas germinadas durante el ensayo
-
NTG: número total de semillas sembradas al inicio del ensayo
Escarificación química (EQ)
Para este ensayo, se utilizaron siete lotes de 50 cipselas obtenidas a partir de diferentes soluciones de ácido sulfúrico (H2SO4), a saber: A) control con H2O destilada, B) H₂SO₄ al 5 % durante 1 min, C) H₂SO₄ al 5 % durante 2 min, D) H₂SO₄ al 10 % durante 1 min, E) H₂SO₄ al 10 % durante 2 min, F) H₂SO₄ al 20 % durante 1 min y G) H₂SO₄ al 20 % durante 2 min. Finalizado el tiempo de exposición, las cipselas fueron lavadas con abundante agua destilada para eliminar los residuos del ácido y evitar daños al embrión. Lo anterior, con el objetivo de desgastar el pericarpo, facilitando un mayor ingreso de agua y el intercambio gaseoso hacia el embrión (Reina et al., 2024; González et al., 2008).
Tratamiento por inmersión térmica (IT)
Se dispusieron tres cajas de Petri, cada una con 50 cipselas distribuidas de manera uniforme. La primera caja se utilizó como grupo control, y, en las demás, las cipselas fueron sumergidas en H2O destilada a 94 °C durante 5 y 50 s. Seguidamente, todas las muestras fueron trasladadas a condiciones controladas de germinación, conforme al protocolo establecido por Sanabria et al. (2001).
Evaluación térmica en ausencia de luz (ETAL)
Se emplearon 50 cipselas por tratamiento en tres cajas de Petri, las cuales fueron incubadas bajo condiciones de oscuridad a tres temperaturas distintas: 4, 23 (control) y 27 °C. El periodo de exposición fue de 20 días, siguiendo el protocolo establecido por Godoi y Takaki (2004).
Exposición a diferentes longitudes de onda (EDLO)
Se usaron 250 semillas, agrupadas en cinco grupos de 50 cipselas por cada caja de Petri, las cuales fueron recubiertas con papel celofán para generar las siguientes condiciones: A) control con luz blanca visible, B) luz roja cercana con celofán rojo (660-680 nm), C) luz roja lejana con celofán rojo y azul (720-740 nm), D) luz azul con celofán azul (380-500 nm) y E) luz amarilla con celofán amarillo (570-581 nm) (Negbi et al., 1968).
Tipología de suelos (TS)
Se usaron cuatro muestras de diferentes suelos, las cuales fueron caracterizadas fisicoquímicamente con base en la metodología del Instituto Geográfico Agustín Codazzi (IGAC, 2006), que a su vez fue utilizada por el Grupo de Investigación de Agroquímica. Se tomó 1 kg de suelo proveniente de la vereda Los Llanos (suelo f) y se caracterizó siguiendo la metodología propuesta por Valdivia y Espinoza (2019). Esta porción de material fue tamizada para retirar raíces, semillas y todo material que interviniera en la germinación. Posteriormente, se utilizaron seis cajas de Petri con 50 cipselas, una de ellas tomadas como muestra control sobre papel filtro, mientras que los tratamientos restantes incluyeron cinco tipos de suelo (Tabla 1, Figura 2).
Nota
: b: suelo b, c: suelo c, d: suelo d, e: suelo e
Tabla 1: Caracterización fisicoquímica de cuatro tipos de suelos del municipio de El Tambo,Cauca, Colombia
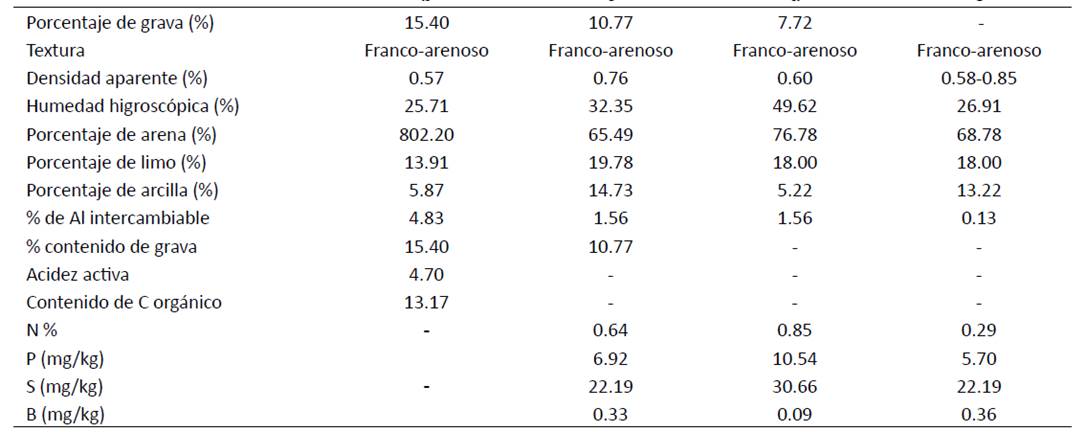
Las muestras de suelo fueron hidratadas con H2O destilada, controlando la aplicación con ayuda de un atomizador. Esto se hizo día de por medio, durante un período de 20 días, a una temperatura ambiente de 24.3°C y con una humedad relativa del 65 %, registrada con un medidor Clock/Humidity HTC-2, en aras de observar la respuesta germinativa con respecto a la disponibilidad de macronutrientes en cada tipo de suelo (Tabla 1, Figura 2).
Registro fotográfico del desarrollo germinativo
Se hizo un fotograma durante 20 días con ayuda del microscopio ECLIPSE Ni-U, con un aumento de 10X, y de un estereoscopio C-DSS115 (ambos de Nikon Corporation, Japón). El seguimiento se hizo sobre el 10 % de una muestra de 300 semillas en cinco tipos de suelo diferentes, con el objetivo de registrar las primeras etapas de germinación y el desarrollo de estructuras como la radícula, el hipocótilo, los cotiledones y el rompimiento del pericarpo. En estas etapas se realizaron mediciones con el software NIS-Elements BR 5.41, mediante la cámara integrada al microscopio y el estereoscopio (Figura 3).
Análisis estadístico
Se utilizaron los programas R 4.5.1 (R Core Team, 2025) y RStudio 2024.12.0 Build 467 (Posit Team, 2025) para realizar pruebas no paramétricas: U de Mann-Whitney para observar diferencias entre semillas viables e inviables, teniendo en cuenta aspectos como la longitud del papus, peso y longitud de la cipsela; Kruskall-Wallis y post hoc de Dunnett para observar diferencias en la prueba de imbibición; y chi cuadrado (X2) para medir variables categóricas como germinada y no germinada en relación con los tratamientos EQ, IT, ETAL, EDLO y TS para comprender si las proporciones de semillas germinadas eran diferentes entre tratamientos. Finalmente, se aplicó la prueba exacta de Fisher para determinar las diferencias significativas entre los diferentes grupos de tratamientos.
RESULTADOS
Viabilidad y capacidad germinativa
Viabilidad y prueba de imbibición
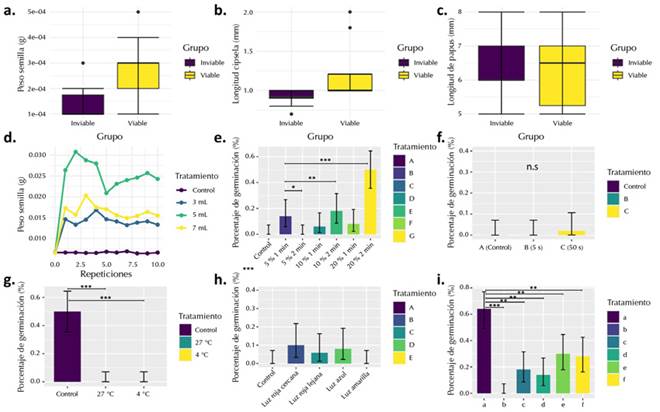
Las semillas evaluadas con TZ mostraron una viabilidad del 100 %, con un valor p < 0.001 para los grupos de aquellas semillas, cuyo peso promedio fue de 0.00028 ± 0.0001 g (Figura 1a), y la longitud de la cipsela con un valor de 1.21 ± 0.4 mm en las semillas viables y 0.92 ± 0.10 mm para las inviables (Figura 1b). No hubo significancia entre la longitud del papus en semillas viables (6.73 ± 1.17 mm) e inviables (6.64 ± 0.95 mm) (Figura 1c). Por lo tanto, este no es un factor determinante para la viabilidad, si bien esta característica del papus, no deja de ser importante en los procesos de dispersión por el viento (anemocoria).
Figura 1: Viabilidad y capacidad germinativa en semillas de P. alopecuroides. a−c) Viabilidad con respecto al peso, la longitud de la cipsela y el papus. d) Prueba de imbibición (3, 5 y 7 mL de H2O) con respecto al peso de la semilla. e) Ensayo de escarificación química. f) Inmersión térmica. g) Evaluación térmica en ausencia de luz. h) Respuesta germinativa a diferentes longitudes de onda. i) Porcentaje de germinación con respecto al tipo de suelos. Nivel de significancia: p < 0.05*, p < 0.01**, p < 0.001***; n.s: no significativo.
Por otro lado, la prueba de imbibición estuvo indirectamente relacionada con las características morfométricas de las semillas de la especie estudiada, donde 5 mL de H2O resultó ser la cantidad óptima requerida para estimular el proceso de absorción en un grupo de diez semillas, observando diferencias significativas entre los tratamientos de 5 y 7 mL (p<0.001) (Figura 1d). Esto incidió en el aumento de peso, con un valor promedio de 0.0239 ± 0.0064 g.
Capacidad germinativa
Escarificación química (EQ)
Para este tratamiento, la concentración óptima de H₂SO₄ fue de 20 %, con un tiempo de exposición de 2 min para 50 semillas viables, cuyo porcentaje de germinación fue de 50 (p<0.001), indicando una relación directa entre el tiempo de exposición y la concentración de H₂SO₄. Las semillas de esta especie herbácea presentan porcentajes de germinación menores al 38 % en concentraciones de 10 % por 2 min (p<0.01) y 5 % por 1 min (p<0.05) (Figura 1e).
Tratamiento por inmersión térmica (IT)
El tratamiento por inmersión en agua, a una temperatura de 94 °C durante 50 s, reportó un 2 % de germinación, así como 0 % después de 5 s (Figura 1f). No se observaron diferencias, comprobando que no hubo estímulo en la germinación ni activación metabólica de la misma. Esto puede deberse a la presencia de fitomelanina, una sustancia que provee de resistencia al pericarpio en cipselas maduras de géneros como Heterocoma, perteneciente a la familia Asteraceae (Mathur et al., 2024).
Evaluación térmica en ausencia de luz (ETAL)
Los cambios de temperatura son factores relevantes en la germinación in situ de las semillas, dado que son condiciones a las cuales se encuentran en ecosistemas de bosque seco tropical y selva subandina de El Tambo. Aquí, Polindara-Moncayo & Sanabria (2022) reportan que el 49 % de las plantas medicinales, entre ellas P. alopecuroides (árnica de loma), crece en espacios soleados como rastrojos, potreros y bordes de carretera, expresando resistencia a periodos de baja precipitación y respondiendo a estímulos de temperatura. En línea con lo anterior, este ensayo demostró que la temperatura óptima de germinación para el 50 % de las semillas en ausencia de luz es de 23 °C (control, p<0.001), y no de 4 y 27 °C, donde el valor reportado fue 0 % (Figura 1g). Se observó un comportamiento fisiológico similar al de Arabidopsis thaliana, para cuya germinación la luz no fue un factor determinante, sino para el crecimiento y el desarrollo vegetativo (Jackson, 2009; Matsoukas, 2014; Roeber et al., 2022). Estos datos indican que temperaturas superiores y/o inferiores a los 23 °C de la muestra control no inducen la ruptura del pericarpo de la cipsela.
Exposición a diferentes longitudes de onda (EDLO)
El 10 % de las semillas germinadas respondió a estímulos de luz roja cercana (630-660 nm), y el 8 % a la luz azul (400-495 nm). Por el contrario, la luz visible (400-700 nm) y la amarilla (600 nm) no presentaron germinación (Figura 1h). Los tratamientos no mostraron diferencias, debido a que son semillas de fotoperiodo neutro, tal como ocurre en especies como Ageratina altissima, Rudbeckia laciniata y Solidago ulmifolia (no fotoblásticas), donde los niveles de luz no influyen en la germinabilidad (Rodrígues de Queiroz & Maricle, 2019).
Tipología de suelos (TS)
En el suelo e, se evidenció una significancia de p < 0.01 con respecto al suelo f, cuyos porcentajes de germinación estuvieron entre el 30 y el 28 %. Por otro lado, se observó un p < 0.001 entre los suelos c y d, con porcentajes de germinación entre el 18 y el 14 % (Figura 1i), en contraste con la muestra control (papel filtro), la germinación fue del 64 %. El suelo f, al presentar un porcentaje de germinación cercano al del suelo e, y no contar con una descripción fisicoquímica, sugiere un TG % y aspectos cualitativos (estructura del suelo, porosidad, color, moteado, presencia de lombrices, compactación y cobertura del suelo) con valores fisicoquímicos semejantes a los del suelo e (Figura 2).
Figura 2: Germinación de Pterocaulon alopecuroides en cinco tipos de suelo: a) muestra control; b) suelo b; c) suelo c; d) suelo d; e) suelo e; f) suelo f, cuyas características fisicoquímicas se encuentran consignadas en la tabla 1; g) hierba fértil, vereda Los Llanos, Tambo, Cauca.
Desarrollo germinativo
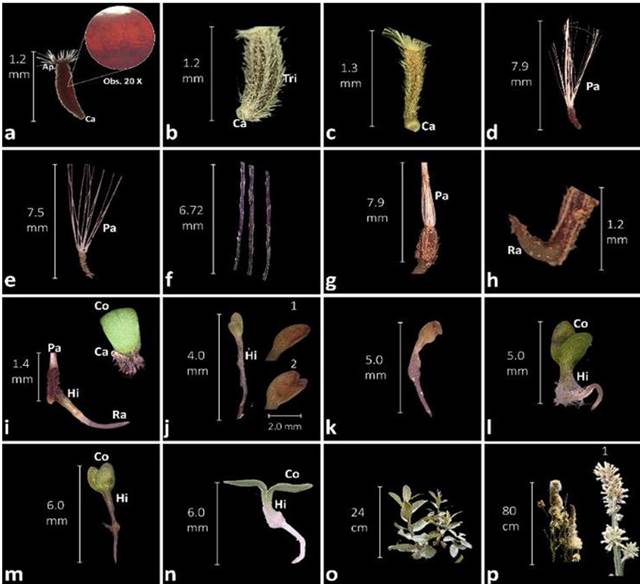
En este estudio se registró la germinación y el desarrollo de P. alopecuroides, que comprenden las siguientes fases en un periodo de 20 días: (i) aparición de la radícula, (ii) crecimiento del hipocótilo, (iii) emergencia y despliegue de los cotiledones, (iv) desarrollo de los primordios foliares y (v) crecimiento de la plántula hasta alcanzar su estado fértil (Figura 3). Estas fases permitieron registrar los cambios morfológicos de la germinación y el desarrollo de las semillas en diferentes tipos de suelo, cuya disponibilidad de macronutrientes influyó en el tiempo de aparición de la radícula y el crecimiento de las estructuras vegetativas.
DISCUSIÓN
La viabilidad refleja el potencial que tiene una semilla para germinar y es un factor determinante en la evaluación de su calidad (Mancipe-Murillo et al., 2018). Por esta razón, en este estudio se aplicaron criterios morfométricos para la selección de cipselas, observándose diferencias significativas entre semillas viables e inviables respecto al peso y la longitud (Figuras 1a y 1b). Sin embargo, la longitud del papus o vilano no fue una característica visual determinante que estuviese asociada a la longitud, el peso y la viabilidad de la cipsela (Figura 1c). Tal fue el caso de los ensayos de germinación en Solidago virgaurea y Solidago niederederi (Pliszko & Kostrakiewicz-Geralt, 2020), donde la eliminación de esta estructura pilosa, asociada a cipselas de longitud de 1.8 a 2.4 mm, no influyó en los mecanismos de germinación de las semillas. Lo contrario ocurrió con Solidago gigantea y Solidago canadensis, donde el desprendimiento del vilano disminuyó el porcentaje final y la velocidad de germinación de las semillas. Lo anterior brinda nuevas perspectivas en torno a la evaluación de los porcentajes y las velocidades de germinación para las cipselas con y sin vilano de distintas especies del género Pterocaulon.
Por consiguiente, la imbibición es un proceso mediado por la permeabilidad y la disponibilidad del agua, con la cual interactúa el pericarpo; estructura que protege los tejidos embrionarios. Estos tejidos son capaces de rehidratarse para reactivar el metabolismo celular y liberar enzimas como las amilasas y las proteasas, responsables de degradar almidones y proteínas que favorecen el crecimiento embrionario (Bewley et al., 2013; Mayer & Poljakoff, 2014; Pompelli et al., 2023). Esta premisa se reafirma en nuestro caso, donde la sustancia responsable de tal protección es la fitomelanina, mostrando una clara diferencia entre semillas viables (marrón-oscuro) e inviables (amarillo) en P. alopecuroides (Figuras 3 b y 3c). Esta sustancia ha sido reconocida como un aspecto de protección y viabilidad en diversas especies de Asteraceae, tal como lo propone Mathur et al. (2024).
Figura 3: Germinación de la semilla y desarrollo de plántulas en Pterocaulon alopecuroides. a) cipsela y glándulas observadas en microscopía de campo claro a 20X; b) cipsela viable; c) cipsela inviable; d) semilla completa viable; e) semilla completa inviable; f) papus blanco-filiforme; g) rompimiento de la testa; h) aparición de la radícula al octavo día; i) crecimiento de la radícula, aparición del hipocótilo y los cotiledones; j) plántula; j1) cotiledones cerrados; j2) cotiledones abiertos; k, l, m) crecimiento radicular, elongamiento del hipocótilo y apertura de los cotiledones; n) despliegue de los cotiledones y emergencia de los primordios foliares; o) plántula a los 180 días; p1) inflorescencia y semillas tipo cipsela a los 365 días. Ca: carpopodium; Tri: tricoma; Pa: papus; Ra: radícula; Hi: Hipocótilo; Co: Cotiledones; Obs. 20X: observación por microscopía óptica de campo claro.
La capa protectora del pericarpo, junto con la evaporación pasiva, contribuyó a minimizar la pérdida de agua durante el proceso de imbibición, donde el volumen de 5 mL mostró los mejores resultados. Se observó un comportamiento fisiológico de absorción y un aumento de peso durante la imbibición, con una diferencia de 0.0173 g en semillas viables de P. alopecuroides. Esto reveló un aumento entre dos y cuatro veces el peso de las semillas, que determina resistencia a la desecación. Tal fue el caso de las semillas ortodoxas de Gaillardia pulchella, de la familia Asteraceae (Bewley, 1997; Doria, 2010; Adegbola & Pérez, 2016).
El tratamiento de 7 mL tuvo efectos negativos como ineficiencia en la imbibición, porque el peso de las semillas era menor, dado que disponían de una mayor cantidad de agua. Esto puede estar relacionado con la saturación en la cipsela (Figura 1d) y la pequeña cantidad de estrías, lo que limitaría la entrada de agua y el intercambio gaseoso necesario para completar las fases posteriores al desarrollo de las plántulas expuestas a déficits hídricos (Navarro García, 2013; Baskin & Baskin, 2023; Pompelli et al., 2023; Mathur et al., 2024).
Entretanto, la escarificación química con H₂SO₄ al 20 % resultó ser el mejor tratamiento; al desgastar el pericarpo, garantizó el ingreso de agua para estimular la germinación. Las semillas respondieron a la irrupción de la latencia por exposición al H₂SO₄ (quimiolatencia) en las cipselas, mostrando tolerancia no solo a la desecación, sino también a la exposición de sustancias alcalinas y ácidas, una propiedad que es otorgada por la fitomelanina presente en el pericarpo (Kiewnick, 1964; Reina et al., 2024), razón por la cual se estudió este tratamiento. No obstante, es importante destacar que las concentraciones elevadas y los tiempos prolongados de exposición son dañinos (Vandana et al., 2020).
El ensayo de IT no presentó diferencias significativas porque ocasionó daños físicos en la estructura del embrión, tal como ocurre en semillas de maíz (González et al., 2014). Paralelamente, la prueba ETAL determinó que la temperatura óptima para la germinación es de 23 °C, alcanzando un 50 % de germinación (Figura 1g). Este resultado permite afirmar que la pérdida de capacidad germinativa está relacionada con la exposición a temperaturas de 4 y 27 °C. Sin embargo, este patrón se observa de manera uniforme en todas las especies de la familia Asteraceae. Por ejemplo, en Tanacetum cinerariifolium, la germinación se ve favorecida por intervalos térmicos específicos, como 25-15, 30-15, 35-20, 15-6 y 20-10 °C (Ilinkin et al., 2020). En especies como Senecio vulgaris se han reportado rangos óptimos de germinación entre 10−25 °C (Popay & Roberts, 1970; Ren, 1991). Esto demuestra que los ensayos pregerminativos basados en variaciones térmicas no son efectivos en todas las especies de esta familia, ya que factores como la variación en la temperatura conllevan cambios en la fisiología de la semilla, sea por un aumento en la turgencia o el rompimiento de la pared celular (Caroca et al., 2016; Szczerba et al., 2021), causando la inhibición o desnaturalización de enzimas antioxidantes como la catalasa y el superóxido dismutasa, que muestran actividad frente al estrés térmico (Guo et al., 2020; Sharma et al., 2022).
La secuencia germinativa de P. alopecuroides (Figura 3) muestra un papus piloso, típico de la familia Asteraceae; estructura que contribuye a su éxito colonizador en hábitats abiertos (Funk et al., 2009), que, en el caso de El Tambo, corresponden a potreros, rastrojos y bordes de carretera, de donde son recolectadas por especialistas de la medicina tradicional. Dichos sabedores han identificado estos espacios como zonas de manejo y fuentes de medicinas herbolarias (Polindara-Moncayo & Sanabria-Diago, 2024). P. alopecuroides es una planta promisoria de valor cultural y terapéutico que exige un registro detallado de su germinación y desarrollo. En este estudio, durante los primeros 20 días, se observó la apertura del pericarpo, la expansión del embrión, la emergencia de los cotiledones, la elongación del hipocótilo y su desarrollo en distintos tipos de suelo a una temperatura de 24.3 °C, con una humedad relativa del 65 % y bajo luz visible. Estas condiciones eran muy cercanas a las del sitio de donde se obtuvieron las semillas, además de ser coherentes con los tratamientos seleccionados (Figuras 3a-3n).
Así, las fases iniciales de la germinación (Figuras 3g-3i) se caracterizaron por el desplazamiento de la radícula y una respuesta a la activación del eje embrionario, mediada por fitohormonas como el ácido giberélico (GA3), responsable del crecimiento vegetativo de las hojas, flores y frutos (Bewley et al., 2013). Se observó un desarrollo emergente y progresivo de los cotiledones verdes en esta especie de la familia Asteraceae (Bakker, 2001).
CONCLUSIONES
El peso, la longitud, y el color marrón-oscuro de la cipsela son características diagnósticas de viabilidad, relacionadas con la capacidad germinativa en semillas y el desarrollo de Pterocaulon alopecuroides. Estos aspectos morfométricos, junto con la cantidad de agua óptima (5 mL) activan la germinación en suelos ácidos y franco-arenosos con una humedad de 26.91 % y la presencia de macronutrientes como N, P, S y B, a una temperatura ambiente de 23 °C como condiciones óptimas para esta especie de importancia biocultural.
Acknowledgements
AGRADECIMIENTOS
Al profesor Giovanni Varona, al profesor Gerardo Andrés Torres de la Unidad de Microscopía, a las profesoras Leidy Tatiana Arcos y Mayra Alejandra Velasco por las asesorías brindadas para el diseño experimental y el análisis estadístico, al profesor Edier Humberto Pérez del Grupo de Agroquímica de la Universidad del Cauca y a la comunidad campesina de la vereda Los Llanos en El Tambo, Cauca.
REFERENCIAS
Licencia
Derechos de autor 2025 Colombia forestal

Esta obra está bajo una licencia internacional Creative Commons Atribución-CompartirIgual 4.0.
Colombia Forestal conserva los derechos patrimoniales (copyright) de las obras publicadas, y favorece y permite la reutilización de las mismas bajo la licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional por lo cual se pueden copiar, usar, difundir, transmitir y exponer públicamente, siempre que:
Se reconozcan los créditos de la obra de la manera especificada por el autor o el licenciante (pero no de una manera que sugiera que tiene su apoyo o que apoyan el uso que hace de su obra).