DOI:
https://doi.org/10.14483/udistrital.jour.colomb.for.2008.1.a08Publicado:
01-01-2008Número:
Vol. 11 Núm. 1 (2008): Enero-DiciembreSección:
Artículos de investigación científica y tecnológicaAnatomía de Madera en 31 Especies de la Subfamilia Mimosoideae (Leguminosae) en Venezuela
Wood anatomy of 31 species from Mimosoideae (Leguminosae) subfamily on Venezuela
Palabras clave:
Mimosoideae, anatomía de la madera, xilema secundario, identificación (es).Palabras clave:
Mimosoideae, wood anatomy, secondary xylem, identification. (en).Descargas
Referencias
apg. 2003. An Update of the Angiosperm Phylogeny Group Classification for the Orders and Families of Flowering Plants. apg ii. Botanical Journal of the Linnean Society 141: 399-436.
Bank, H. & P. Gasson. 2000. Pollen Morphology and Wood Anatomy of the Crudia Group (Leguminosae, Caesalpinoideae, Detarieae). Botanical Journal of the Linnean Society 134: 19-59.
Barajas, J. & C. León. 1989. Anatomía de maderas de México: especies de una selva baja caducifolia. Universidad Nacional Autónoma de México. Instituto de Biología. Publicaciones especiales 16. México D.F. Pg. 126.
Barajas, M., G. Ángeles & P. Solís. 1997. Anatomía de maderas de México: especies de una selva alta perennifolia I. Universidad Nacional Autónoma de México. Instituto de Biología. Publicaciones especiales 16. México D.F. Pg. 126.
Baretta-Kuipers, T. 1979. Wood Anatomy of Archidendron F. v. Mueller, Mimosoideae, Leguminosae. iawa Bulletin 2/3: 47-50.
Baretta-Kuipers, T. 1981. Wood Anatomy of Leguminosae: Its Relevance to Taxonomy. En: Polhill, R. & P. Raven (eds.). Advances in Legume Systematics: 677-705.
Castro, A., J. Alves & F. Vasconcellos. 1992. Ocorrencia de fibres lenhosas septadas em madeiras da Amazonia. Boletim do Museu Paraense Emilio Goeldi. Botánica 8: 191-201.
Chauhan, L. & R. Dayal. 1985. Wood Anatomy of the Indian Albizias. iawa Bulletin 6: 213218.
Corothie, H. 1967. Estructura anatómica de 47 maderas de la Guayana venezolana. Laboratorio Nacional de Productos Forestales. Universidad de Los Andes yMinisterio de Agricultura y Cría. Mérida, Venezuela.
Cronquist, A. 1981. An Integrated System of Classification of Flowering Plants. Columbia University Press. NewYork. Pg. 1262.
Cumbie, B. 1960. Anatomical Studies on the Leguminosae. Tropical Woods 113: 1-47.
Espinoza de P., N. & W. León H. 2003. Estudio anatómico del leño de 56 especies de la subfamilia Papilionoideae (Leguminosae) de Venezuela. Consejo de Desarrollo Científico, Humanístico y Tecnológico. Universidad de Los Andes. Mérida, Venezuela. Pg. 145.
Espinoza de P., N. & J. Melandri. 2000. Estudio anatómico del leño de cinco especies de la subfamilia Mimosoideae en Venezuela. Revista Pittieria 29/30: 75-88.
Espinoza de P., N. & J. Melandri. 2006. Anatomía de la madera de 68 especies de la subfamilia Caesalpinoideae (Leguminosae) en Venezuela. Consejo de Desarrollo Científico, Humanístico y Tecnológico. Universidad de Los Andes. Mérida, Venezuela. Pg. 189.
Evans, J. A., P. E. Gasson, & G. P. Lewis. 2006. Wood Anatomy of the Mimosoideae (Leguminosae). iawa Journal. Supplement 5. Pg. 117.
Gasson, P. 1996. Wood Anatomy of the Tribe Swartzieae with Comments on Related Papilionoid and Caesalpinioid Leguminosae. iawa Journal 17: 45-75.
Gasson, P. 1999. Wood Anatomy of the Tribe Dipterygeae with Comments on Related Papilionoid and Caesalpinoid Leguminosae. iawa Journal 20: 441-455.
Gasson, P. 2000. Does Wood Anatomy Support Tribal and Generic Classification in Papilionoideae-Leguminosae? En Herenden P.& A. Bruneau (eds.). Advances in Legume Systematics Part 9: 201-215.
Höhn, A. 1999. Wood Anatomy of Selected West African Species of Caesalpinoideae and Mimosoideae (Leguminosae): A Comparative Study. iawa Journal 20: 115-146.
iawa Committee. 1989. iawa List of Microscopic Features for Hardwood Identification. iawa Bulletin 10: 219-332.
Inside Wood. 2008. [Disponible en: http://insidewood/ lib.ncsu.edu/search, consultado en marzo de 2008].
junac. 1981. Descripción general y anatómica de 105 maderas del grupo andino. Junta del Acuerdo de Cartagena. Lima.
Kribs, D. 1968. Commercial Foreign Woods in the American Market. Dover Publications New York.
Loureiro, A. & M. Da Silva. 1981. Estudo dendrológico e anatômico do lenho de 7 espécies e 3 subespécies de Dimorphandra (Leguminosae-Caesalpinoideae). Acta Amazonica 13: 149-170.
Loureiro, A., F. Vasconcellos & M. Da Silva. 1983. Contribuçao ao estudo anatômico do lenho de 5 espécies de Sclerolobium e 5 espécies de Tachigalia (Leguminosae) da Amazónia. Acta Amazonica 13: 149-170.
Mabberley, D. 1990. The Plant Book. Cambridge University Press. New York.
Mainieri, C. & J. Peres. 1989. Fichas de caracteristicas das madeiras brasileiras. Instituto de Pesquisas Tropicales. Sao Paulo.
Metcalfe, C. & L. Chalk. 1950. Anatomy of the Dicotyledons Vol. I. Oxford University Press. Oxford.
Miller, R. & P. Détienne. 2001. Major Timber Trees of Guyana. Wood Anatomy. Tropenbos International. Wageningen, Holanda.
Nardi, R. & M. Edlmann. 1992. Legnami tropicali importati in Italia: Anatomia e identificazione. Vol. II: America Latina. Istituto di Assestamento e Tecnología Forestale. Universita di Firenze. Florencia.
Paula, J. de 2003. Caracterizaçao anatômica da madeira de sete espécies da Amazônia con vistas a produção de energia e papel. Acata Amazonica 33: 243-266.
Record, S. & R. Hess. 1949. Timbers of the New World. Yale University Press. Cuarta edición. New Haven, Connecticut.
Cómo citar
APA
ACM
ACS
ABNT
Chicago
Harvard
IEEE
MLA
Turabian
Vancouver
Descargar cita
 |
León-H., W.J. (2008). Anatomía de madera en 31 especies de la subfamilia Mimosoideae (Leguminosae) en Venezuela. Colombia Forestal, 11, 113-136. |
ANATOMÍA DE MADERA EN 31 ESPECIES DE LA SUBFAMILIA MIMOSOIDEAE (LEGUMINOSAE) EN VENEZUELA
Anatomy of 31 species from Mimosoideae (Leguminosae) subfamily on Venezuela
Anatomia de madiera em 31 especies da subfamília Mimosoideae (Leguminosae) na Venezuela
Williams J. León H.1
1Universidad de Los Andes, Mérida, Venezuela, wleon@ula.ve.
Recepción: Junio 23 de 2008/Aprobación: Julio 18 de 2008
RESUMEN
El presente trabajo tiene como objetivo estudiar la anatomía de la madera de 31 especies, correspondientes a 17 géneros, de la subfamilia Mimosoideae (Leguminosae), procedentes de diferentes regiones geográficas de Venezuela. Se estudiaron entre uno y cinco individuos por especie. Las descripciones se realizaron siguiendo lo estipulado por el IAWA Committee (1989). Las especies estudiadas se pueden dividir en dos grandes grupos, de acuerdo a la presencia o ausencia de fibras septadas. El género Inga se caracterizó porque todas las especies estudiadas presentaron fibras septadas, mientras que Albizia y Enterolobium presentaron especies con fibras septadas y especies con fibras no septadas. Las características cuantitativas de los vasos y el ancho de radio mostraron suficiente variación como para ser consideradas características importantes desde el punto de vista taxonómico. El parénquima predominantemente fue de tipo paratraqueal vasicéntrico ancho, aliforme de ala corta y confluente. En Calliandra laxa, Prosopis juliflora y Zygia longifolia predominó el parénquima en bandas anchas; mientras que en Cedrelinga cateniformis el parénquima predominantemente fue paratraqueal vasicéntrico delgado. Todas las especies, con la excepción de Cedrelinga cateniformis, presentaron cristales prismáticos en las células parenquimáticas axiales. A pesar de encontrar cierta uniformidad anatómica, se logró elaborar una clave para la identificación de las especies estudiadas.
Palabras clave: Mimosoideae, anatomía de la madera, xilema secundario, identificación.
ABSTRACT
This paper is about the wood anatomy of 31 species, belonging to 17 genera, of the Mimosoideae subfamily (Leguminosae), proceeding from different geographical regions of Venezuela. For each species, one to five individuals were studied. The descriptions were realized according to the IAWA Committee(1989). The studied species may be divided in two groups according to the presence or absence of septate fibers. All species of Inga showed septate fibers, whereas Albizia and Enterolobium included species with septate fibers and also species with non-septate fibers. The quantitative characteristics of the vessels and the width of rays showed sufficient variation as to be considered important characteristics from ataxonomic point of view. The most common parenchyma type was vasicetric, aliform and confluent. In Calliandra laxa, Prosopis juliflora and Zygia longifolia the main parenchyma type was in wide bands; whereas in Cedrelinga cateniformis, the main parenchyma type was thin vasicentric. All species studied, with the exception of Cedrelinga cateniformis, presented prismatic crystals in the parenchymatous axials cells. In spite of finding certain anatomical uniformity, it was possible to elaborate a key for the identification of the studied species.
Key Words: Mimosoideae, wood anatomy, secondary xylem, identification.
RESUMO
O presente trabalho tem como objetivo estudar a anatomia da madeira de 31 espécies, correspondentes a 17 gêneros, da subfamília Mimosoideae (Leguminosae), procedentes de diferentes regiões geográficas da Venezuela. Se estudiaram entre uno e cinco indivíduos por espécie. As descrições se realizaram seguindo o estipulado pelo i awa Committee (1989). As espécies estudadas se puedem dividir em dois grandes grupos, de acordo com a presença ou ausência de fibras septadas. O gênero Inga se caracterizou porque todas as espécies estudadas apresentaram fibras septadas, enquanto que Albizia e Enterolobium apresentaram espécies com fibras septadas e espécies com fibras não septadas. As características quantitativas dos vasos e a largura do rádio mostraram suficiente variação para serem consideradas características importantes desde o ponto de vista taxonômico. O parênquima predominante foi do tipo paratraqueal vasicêntrico largo, em forma de asa curta e confluente. Na Calliandra laxa, Prosopis juliflora e Zygia longifolia predominou o parênquima em bandas largas; enquanto que na Cedrelinga cateniformis o parênquima predominante foi o paratraqueal vasicêntrico fino. Todas as espécies, com a esceção da Cedrelinga cateniformis, apresentaram cristais prismáticos nas células parenquimáticas axiais. Apesar de encontrar certa uniformidade anatómica, conseguiu-se elaborar uma chave para a identificação das espécies estudadas.
Palavras chave: Mimosoideae, anatomia da madeira, xilema secundário, identificação.
INTRODUCCIÓN
La familia Fabaceae (Leguminosae) pertenece al orden Fabales y está constituida por más de 600 géneros y 16000 especies de hierbas, arbustos, árboles y lianas, las cuales se encuentran incluidas en tres subfamilias: Caesalpinoideae, Mimosoideae y Papilionoideae (Mabberley 1990). Algunos sistemas de clasificación le dan rango de familia a las tres subfamilias mencionadas; sin embargo sistemas recientes como APG (2003) mantienen el criterio de considerarla como una sola familia. La Mimosoideae es la subfamilia menos numerosa de las Leguminosae; según Mabberley (1990) incluye cerca de 60 géneros y más de 3000 especies. Desde el punto de vista económico, son muchas las especies de valor comercial, bien sea por la calidad de su madera, como plantas alimenticias o medicinales. Con relación a la anatomía de maderas, son muchos los estudios que presentan información a nivel de especies, pero muchas veces en trabajos donde combinan diferentes grupos taxonómicos (Kribs 1968, JUNAC 1981, Barajas & León 1989, Mainieri & Peres 1989, Nardi & Edlmann 1992, Barajas et al. 1997, Miller & Détienne 2001). También destacan las descripciones a nivel de familia o subfamilia presentadas por Record & Hess (1949), Metcalfe & Chalk (1950), Cumbie (1960), Baretta-Kuipers (1981) y Evans, Gasson & Lewis (2006); así como dentro de algunas tribus, subtribus o géneros pertenecientes a las diferentes subfamilias de las Leguminosae (Baretta-Kuipers 1979, 1981, Loureiro & da Silva 1981, Loureiro et al. 1983, Chauhan & Dayal 1985, Höhn 1999, Bank & Gasson 2000, Gasson 1994, 1996 ,1999, 2000). En Venezuela se han realizado trabajos de gran importancia para las subfamilias Caesalpinoideae (Espinoza de P. & Melandri 2006) y Papilionoideae (Espinoza de P. & León 2003). Dentro de la subfamilia Mimosoideae se ha presentado la descripción de algunas especies en Venezuela y se pueden mencionar las realizadas por Espinoza de P. y Melandri (2000), Pérez (1971) y Corothie (1967).
Son muchas las especies de la subfamilia Mimosoideae importantes en Venezuela: desde el punto de vista maderero, Samanea saman ha sido ampliamente utilizada en la industria de la construcción y del mueble; como árboles emblemáticos se tienen a las especies Prosopis juliflora (estado Falcón) y Samanea saman (estado Aragua); muchas especies del género Inga son utilizadas como árbol de sombra para cultivos agrícolas. Sin embargo, a pesar de su importancia, hasta el presente sólo se ha realizado un estudio anatómico que concentre únicamente especies de este grupo taxonómico y fue el realizado por Espinoza de P. & Melandri (2000), donde describen cinco especies. Por esta razón, el presente trabajo tiene como objetivos describir la anatomía xilemática de 31 especies de la subfamilia Mimosoideae que crecen en diferentes localidades de Venezuela y elaborar una clave dicotómica para la identificación de las mismas.
MATERIALES Y MÉTODOS
El material de estudio está constituido por muestras de madera de 31 especies, pertenecientes a 17 géneros, de la subfamilia Mimosoideae colectadas en diferentes regiones de Venezuela y accedidas en la xiloteca MERW (Tabla 1) del Laboratorio de Anatomía de Maderas de la Universidad de Los Andes (Mérida, Venezuela). Se extrajeron cubos de madera y fueron sometidos a un proceso de ablandamiento en agua caliente durante 4-32 horas, dependiendo del grado de dureza de la madera. Posteriormente se realizó el proceso de corte con un microtomo de deslizamiento para obtener secciones de 20-30 µm de espesor. Para la tinción se utilizó safranina y finalmente, se procedió a la deshidratación, montaje y rotulado del material para estudio microscópico. En la preparación de macerados se sumergieron astillas en una solución de peróxido de hidrógeno y ácido acético glacial (1:1) para ser llevadas a estufa (12 horas, 60 ºC) y, posterior a la individualización de fibras y elementos vasculares, se realizó la coloración con safranina y el montaje, utilizando bálsamo de Canadá. Para la descripción se siguió lo estipulado por el IAWA Committee (1989), tanto en características cualitativas como cuantitativas. En la toma de fotomicrografías se utilizó una cámara Pentax SX-n acoplada a un microscopio Leica (Modelo Gallen III).
RESULTADOS
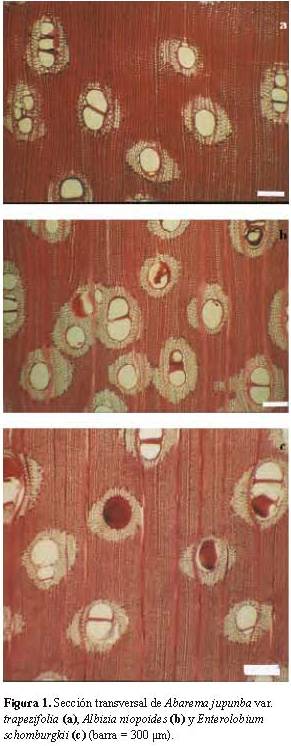
Abarema jupunba var. trapezifolia (Vahl) Barneby & J. W. Grimes. (Figura 1a); A. villifera (Ducke) Barneby & J. W. Grimes
Madera con albura de color amarillo claro, sin transición entre albura y duramen. Olor y sabor no distintivo. Lustre mediano. Grano inclinado a entrecruzado. Textura mediana. Moderadamente dura y pesada.
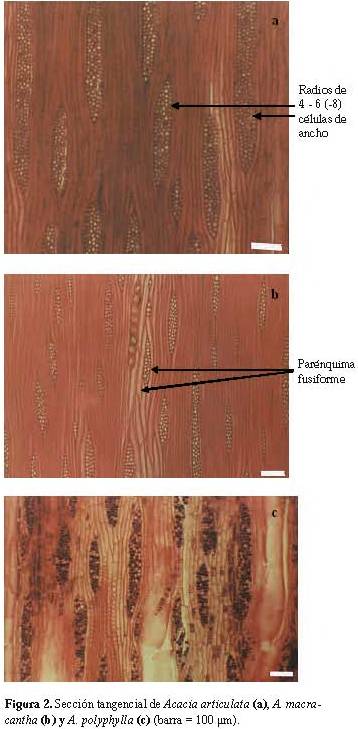
Anillos de crecimiento no definidos. Porosidad difusa. Poros sin patrón definido de disposición, solitarios y múltiples radiales de 2-3 (-8). Platinas de perforación simples. Punteaduras intervasculares alternas, circulares a ovaladas, diminutas a pequeñas, ornadas. Punteaduras radiovasculares similares a las intervasculares. Depósitos de goma presentes. Fibras no septadas, paredes exclusivamente delgadas (A. villifera) o delgadas a medianas (A. jupunba var. trapezifolia), punteaduras indistintamente areoladas. Parénquima apotraqueal difuso (A. jupunba var. trapezifolia), ocasionalmente en islas dispersas (X6503, X6520), paratraqueal vasicéntrico ancho, aliforme de ala corta, confluente, fusiforme y en series de 2-4 células; ocasionalmente hasta 6 células en A. jupunba var. trapezifolia. Radios homocelulares de células procumbentes. Cristales prismáticos en series parenquimáticas cristalíferas, largas y abundantes, ocasionalmente algunas cámaras vacías (A. jupunba var. trapezifolia); un cristal por cámara, ocasionalmente 2.Acacia articulata Ducke (Figura 2a); A. macracantha Humb. & Bonpl. ex Willd (Figura 2b); A. polyphylla DC (Figura 2c).
Madera con albura amarilla a blanco-amarillento; duramen color marrón con transición abrupta albura-duramen (A. macracantha). Olor y sabor no distintivo. Lustre mediano. Grano recto a inclinado. Textura mediana. Moderadamente dura y pesada a dura y pesada.
Anillos de crecimiento indistintos (A. articulata) a definidos por reducción del diámetro radial de las fibras (A. macracantha) o parénquima marginal (A. polyphylla). Porosidad difusa. Poros sin patrón definido de disposición, solitarios y múltiples radiales de 2-3 (-5), algunos arracimados, platinas de perforación simples. Punteaduras intervasculares alternas, circulares a ovaladas y poligonales, pequeñas a medianas, ornadas (A. polyphylla). Punteaduras radiovasculares similares a las intervasculares. Fibras no septadas, paredes medianas a gruesas. Parénquima paratraqueal vasicéntrico ancho, aliforme de ala corta, confluente; marginal (A. polyphylla); fusiforme (A. macracantha, A. polyphylla) y en series de 2-4 células; hasta 7 células en A. articulata. Radios homocelulares de células procumbentes. Cristales prismáticos en series parenquimáticas cristalíferas, largas y abundantes, pudiendo llegar a formar idioblastos (A. macracantha); un cristal por cámara.
Albizia niopoides (Spruce ex Benth.) Burkart. (Figura 1b); A. pistaciifolia Barneby & J.W. Grimes.Madera con albura de color amarillo, sin transición entre albura y duramen. Olor y sabor no distintivo. Lustre bajo. Grano inclinado a entrecruzado. Textura mediana. Moderadamente dura y pesada a dura y pesada.
Anillos de crecimiento indistintos a ligeramente definidos por reducción del diámetro radial de las fibras (A. niopoides, X3530). Porosidad difusa. Poros sin patrón definido de disposición, solitarios y múltiples radiales de 2-3 (-6), algunos arracimados. Platinas de perforación simples. Punteaduras intervasculares alternas, circulares a ovaladas, aberturas coalescentes, diminutas a pequeñas en A. niopoides, pequeñas a medianas en A. pistaciifolia, ornadas. Punteaduras radiovasculares similares a las intervasculares. Fibras septadas y no septadas (A. niopoides) a exclusivamente no septadas (A. pistaciifolia), paredes medianas a gruesas, punteaduras indistintamente areoladas. Parénquima paratraqueal vasicéntrico ancho, aliforme de ala corta, confluente; en series de 2-4 (-6) células. Radios homocelulares de células procumbentes. Cristales prismáticos en series parenquimáticas cristalíferas, largas y abundantes; un cristal por cámara.
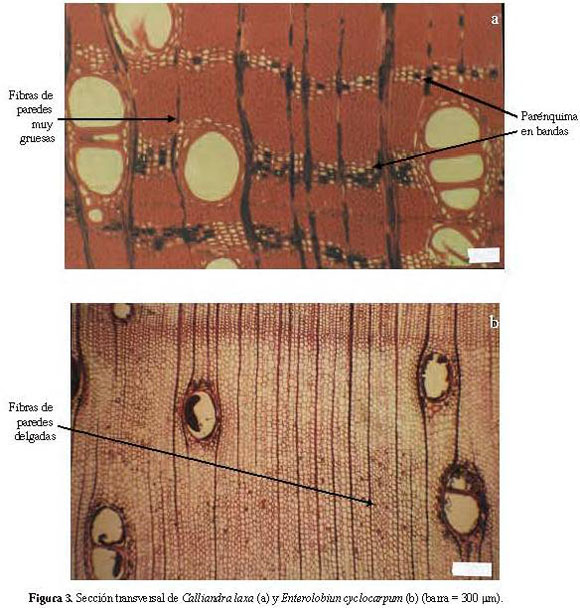
Calliandra laxa (Willd.) Benth. (Figura 3a).
Madera de color marrón claro, sin transición entre albura y duramen. Olor y sabor no distintivo. Lustre bajo. Grano inclinado a entrecruzado. Textura mediana. Dura y pesada.
Anillos de crecimiento ligeramente definidos por reducción del diámetro radial de las fibras y bandas cristalíferas de parénquima. Porosidad difusa. Poros sin patrón definido de disposición, solitarios y múltiples radiales de 2-5, arracimados. Platinas de perforación simples. Punteaduras intervasculares alternas, circulares a ovaladas, diminutas, ornadas. Punteaduras radiovasculares similares a las intervasculares. Fibras no septadas, paredes muy gruesas, punteaduras indistintamente areoladas. Parénquima en bandas con más de tres células de ancho; en series de 2-4 células. Radios homocelulares de células procumbentes. Cristales prismáticos en series parenquimáticas cristalíferas, largas y abundantes; un cristal por cámara.
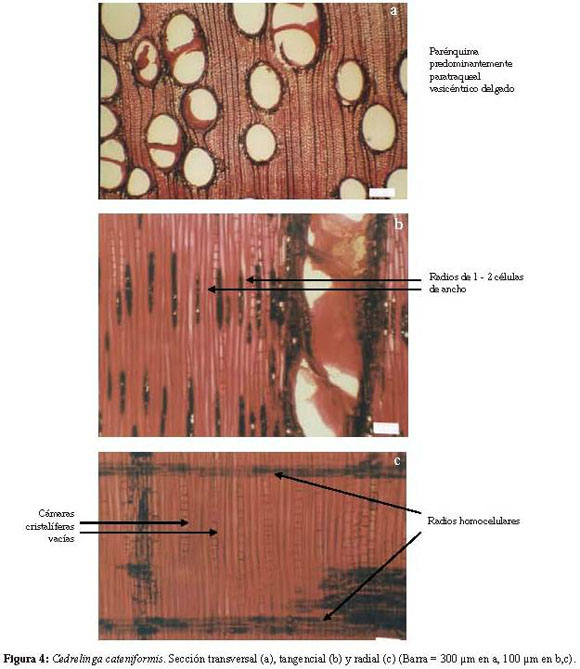
Cedrelinga cateniformis (Ducke) Ducke. (Figura 4a, 4b y 4c).
Madera de color marrón claro, sin transición entre albura y duramen. Olor y sabor no distintivo. Lustre mediano a alto. Grano inclinado a entrecruzado. Textura mediana a gruesa. Moderadamente dura y pesada.
Anillos de crecimiento indistintos. Porosidad difusa. Poros sin patrón definido de disposición, solitarios y múltiples radiales de 2-4 (-7). Platinas de perforación simples. Punteaduras intervasculares alternas, circulares a ovaladas, medianas a grandes, ornadas. Punteaduras radiovasculares similares a las intervasculares. Depósitos de goma en los poros. Fibras no septadas, paredes delgadas, punteaduras indistintamente areoladas. Parénquima apotraqueal difuso y, predominantemente, paratraqueal vasicéntrico delgado; en series de 4-5 (-8) células. Radios homocelulares de células procumbentes. Cristales ausentes, abundantes cámaras vacías en parénquima axial.
Enterolobium cyclocarpum (Jacq.) Griseb. (Figura 3b); E. schomburgkii Benth. (Figura 1c).
Madera con albura de color amarillo. Olor y sabor no distintivo. Lustre bajo a mediano. Grano recto a inclinado (E. cyclocarpum) a entrecruzado (E. schomburgkii). Textura mediana. Blanda y liviana (E. cyclocarpum) hasta muy dura y pesada (E. schomburgkii).
Anillos de crecimiento indistintos (E. cyclocarpum) o definidos por estrechas zonas donde se presenta una reducción del diámetro radial de las fibras (E. schomburgkii). Porosidad difusa. Poros sin patrón definido de disposición, en E. cyclocarpum solitarios y múltiples radiales de 2, predominantemente solitarios; en E. schomburgkii solitarios y múltiples radiales de 2-3 (-5). Platinas de perforación simples. Punteaduras intervasculares alternas, circulares a ovaladas, medianas en E. cyclocarpum, diminutas a pequeñas en E. schomburgkii, ornadas. Punteaduras radiovasculares similares a las intervasculares. Depósitos de goma en los poros. Fibras no septadas, paredes muy delgadas (E. cyclocarpum, X2690), delgadas a medianas (E. cyclocarpum, X6363) y gruesas a muy gruesas (E. schomburgkii), punteaduras indistintamente areoladas. Parénquima apotraqueal difuso (E. schomburgkii, poco), paratraqueal vasicéntrico ancho, confluente; en series de 2-4 células; ocasionalmente hasta 6 células (E. schomburgkii). Radios homocelulares de células procumbentes. Cristales prismáticos en series parenquimáticas cristalíferas, largas, abundantes; algunas cámaras vacías (E. schomburgkii).
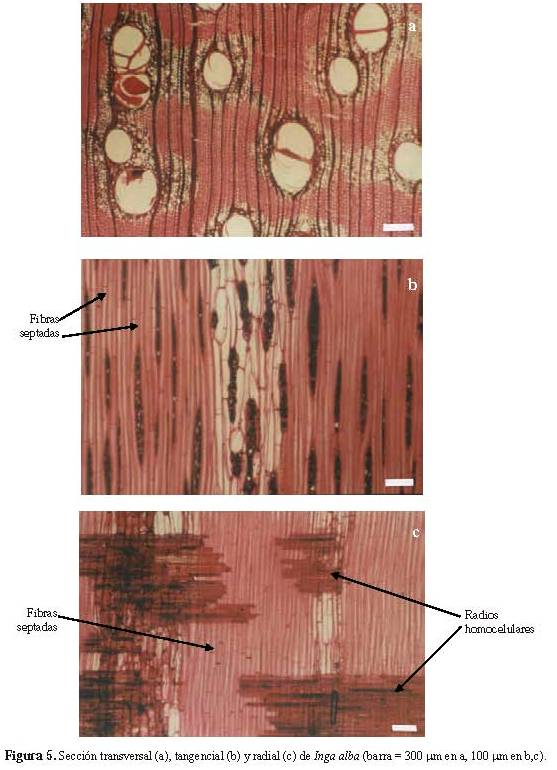
Inga alba (Sw.) Willd. (Figura 5a, 5b y 5c); I. edulis Mart.; I. ingoides (Rich.) Willd.; I. laurina (Sw.) Willd.; I. oerstediana, Benth.; I. splendens, Willd.
Madera con albura de color amarillo, amarillo claro a crema rosáceo, sin transición entre albura y duramen en I. edulis, I. ingoides, I. laurina e I. oerstediana; duramen marrón a marrón claro en I. alba e I. splendens. Olor y sabor no distintivo. Lustre mediano. Grano recto a inclinado (I. alba, I. edulis I. splendens), entrecruzado (I. alba, I. ingoides, I. laurina, I. oerstediana). Textura mediana. Moderadamente dura y pesada (I. alba, I. splendens) a dura y pesada (I. laurina, I. oerstediana) o blanda y liviana (I. ingoides) a moderadamente dura y pesada (I. edulis).
Anillos de crecimiento indistintos a ocasionalmente definidos por reducción de diámetro radial de las fibras y presencia de banda parenquimática cristalífera (I. ingoides). Porosidad difusa. Poros sin patrón definido de disposición, solitarios y múltiples radiales de 2-3 (-5-8), ocasionalmente arracimados. Platinas de perforación simples. Punteaduras intervasculares alternas, circulares a ovaladas, ocasionalmente con aberturas coalescentes, pequeñas a medianas, ornadas. Punteaduras radiovasculares similares a las intervasculares. Depósitos de goma en los poros. Fibras comúnmente septadas; septadas y no septadas en I. laurina, paredes delgadas a medianas en I. alba, I. edulis, I. ingoides, delgadas a gruesas en I. oerstediana, medianas a ocasionalmente gruesas en I. splendens y exclusivamente gruesas en I. laurina, punteaduras indistintamente areoladas. Parénquima apotraqueal difuso (I. alba, X5924) y en islas dispersas (I. alba, I. ingoides, I. splendens), paratraqueal vasicéntrico ancho, aliforme de ala corta, confluente; fusiforme (poco) y series de 2-4 (-5) células. Radios homocelulares de células procumbentes. Cristales prismáticos formando series parenquimáticas cristalíferas largas y desde pocas hasta abundantes.
Newtonia psilostachya (DC) Brenan
Madera con albura marrón amarillenta y duramen marrón, transición abrupta entre albura y duramen. Olor y sabor no distintivo. Lustre mediano a alto. Grano entrecruzado. Textura fina. Dura y pesada.
Anillos de crecimiento definidos por reducción del diámetro radial y engrosamiento de las paredes de las fibras. Porosidad difusa. Poros sin patrón definido de disposición, solitarios y múltiples radiales de 2-3 (-5), ocasionalmente arracimados. Platinas de perforación simples. Punteaduras intervasculares alternas, circulares a ovaladas, pequeñas a medianas, ornadas. Punteaduras radiovasculares similares a las intervasculares. Depósitos de goma presentes. Fibras no septadas, paredes medianas a gruesas, punteaduras indistintamente areoladas. Parénquima paratraqueal vasicéntrico ancho, aliforme de ala corta, confluente, unilateral, ocasionalmente apotraqueal difuso (X3896), en series de 2-4 células. Radios homocelulares de células procumbentes. Cristales prismáticos en series parenquimáticas cristalíferas, largas y abundantes; un cristal por cámara.
Parkia nitida Miq.; P. pendula (Willd.) Benth. ex Walp.
Madera de color amarillo, sin transición entre albura y duramen. Olor y sabor no distintivo. Lustre mediano a alto. Grano recto a inclinado. Textura mediana. Blanda y liviana.
Anillos de crecimiento definidos (P. pendula) a ligeramente definidos (P. nitida) por estrecha zona con reducción de diámetro radial de las fibras. Porosidad difusa. Poros sin patrón definido de disposición, solitarios y múltiples radiales de 2-3, algunos arracimados (P. nitida). Platinas de perforación simples. Punteaduras intervasculares alternas, circulares a ovaladas, medianas, ornadas. Punteaduras radiovasculares similares a las intervasculares. Depósitos de goma en los poros. Fibras no septadas, paredes muy delgadas (P. nitida) a delgadas (P. pendula), punteaduras indistintamente areoladas. Parénquima apotraqueal difuso (P. nitida), paratraqueal vasicéntrico ancho, aliforme de ala corta, confluente, fusiforme (poco, P. nitida) y en series de 2-4 células (P. nitida) o (2-) 4-6 células (P. pendula). Radios homocelulares de células procumbentes. Cristales prismáticos en series parenquimáticas cristalíferas, largas y abundantes, principalmente en el parénquima difuso; un cristal por cámara.
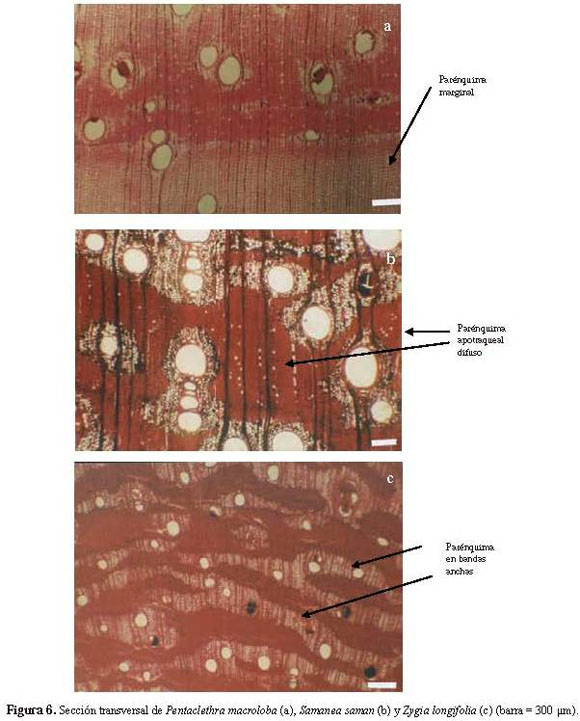
Pentaclethra macroloba (Willd.) Kuntze (Figura 6a).
Madera con albura de color amarillo y duramen marrón, transición abrupta entre albura y duramen. Olor y sabor no distintivo. Lustre mediano. Grano recto. Textura fina a mediana. Moderadamente dura y pesada a dura y pesada.
Anillos de crecimiento definidos por parénquima marginal, reducción del diámetro radial y engrosamiento de las paredes de las fibras. Porosidad difusa. Poros sin patrón definido de disposición, solitarios y múltiples radiales de 2-3 (-6), ocasionalmente arracimados. Platinas de perforación simples. Punteaduras intervasculares alternas, circulares a ovaladas, diminutas a pequeñas, ornadas. Punteaduras radiovasculares similares a las intervasculares. Depósitos de goma presentes. Fibras no septadas, paredes delgadas a gruesas, punteaduras indistintamente areoladas. Parénquima apotraqueal difuso con algunas islas apotraqueales dispersas, paratraqueal vasicéntrico ancho, aliforme de ala corta, confluente, marginal, fusiforme y en series de 2-4 (-6) células. Radios homocelulares de células procumbentes. Cristales prismáticos en series parenquimáticas cristalíferas, largas y abundantes; un cristal por cámara.
Piptadenia leucoxylon Barneby & J. W. Grimes.
Madera de color amarillo, sin transición entre albura y duramen. Olor y sabor no distintivo. Lustre bajo. Grano recto a inclinado. Textura fina. Moderadamente dura y pesada.
Anillos de crecimiento definidos por reducción del diámetro radial y engrosamiento de las paredes de las fibras junto con estrechas y discontinuas bandas de parénquima marginal. Porosidad difusa. Poros sin patrón definido de disposición, solitarios y múltiples radiales de 2-5 (-7), arracimados. Platinas de perforación simples. Punteaduras intervasculares alternas, circulares a ovaladas, pequeñas a medianas, no ornadas. Punteaduras radiovasculares similares a las intervasculares. Fibras no septadas, paredes medianas a gruesas, punteaduras indistintamente areoladas. Parénquima paratraqueal vasicéntrico ancho, aliforme de ala corta, confluente, unilateral, estrechas bandas marginales, fusiforme y en series de 2-4 células. Radios homocelulares de células procumbentes. Cristales prismáticos en series parenquimáticas cristalíferas, largas y abundantes; un cristal por cámara.
Pithecellobium dulce (Roxb.) Benth.; P. jupunba (Willd.) Urb.; P. pedicellare (DC.) Benth.; P. roseum (Vahl) Barneby & J. W. Grimes
Madera con albura crema amarillento a crema rosáceo y duramen marrón rojizo, transición gradual entre albura y duramen en P. pedicellare y abrupta en P. dulce y P. roseum. Olor y sabor no distintivo. Lustre mediano a alto. Grano recto a inclinado o entrecruzado (P. jupunba, P. roseum). Textura mediana. Moderadamente dura y pesada a dura y pesada; blanda y liviana en P. jupunba.
Anillos de crecimiento indistintos a definidos por reducción del diámetro radial de las fibras. Porosidad difusa. Poros sin patrón definido de disposición, solitarios y múltiples radiales de 2; hasta 3 en P. dulce, P. jupunba, P. pedicellare y hasta 4 en P. roseum. Platinas de perforación simples. Punteaduras intervasculares alternas, circulares a ovaladas, ocasionalmente poligonales en P. dulce, diminutas en P. pedicellare y P. jupunba, y medianas en P. dulce, P. roseum; ornadas. Punteaduras radiovasculares similares a las intervasculares. Fibras no septadas, paredes delgadas en P. jupunba, delgadas a moderadamente gruesas en P. pedicellare, medianas a gruesas en P. dulce, gruesas a muy gruesas en P. roseum; punteaduras indistintamente areoladas. Parénquima paratraqueal vasicéntrico ancho, aliforme de ala corta, confluente, ocasionalmente algunas islas apotraqueales dispersas (P. dulce, X4792), unilateral y bandas anchas en P. roseum; fusiforme y en series de 2-4 células. Radios homocelulares de células procumbentes. Cristales prismáticos en series parenquimáticas cristalíferas, largas y abundantes; un cristal por cámara; ocasionalmente 2 (P. jupunba).
Prosopis juliflora (Sw.) DC
Madera con albura amarilla y duramen marrón oscuro. Olor y sabor no distintivo. Lustre mediano. Grano entrecruzado. Textura fina a mediana. Dura y pesada a muy dura y pesada.
Anillos de crecimiento no definidos. Porosidad difusa. Poros sin patrón definido de disposición, solitarios y múltiples radiales de 2-4, arracimados. Platinas de perforación simples. Punteaduras intervasculares alternas, circulares a ovaladas, pequeñas a medianas, no ornadas. Punteaduras radiovasculares similares a las intervasculares. Depósitos de goma presentes. Fibras no septadas, paredes muy gruesas, punteaduras indistintamente areoladas. Parénquima apotraqueal difuso (poco), paratraqueal aliforme de ala corta, confluente, predominantemente en bandas con más de tres células de ancho, fusiforme (abundante) y en series de 2 (-4) células. Radios homocelulares de células procumbentes. Cristales prismáticos en series parenquimáticas cristalíferas, largas y abundantes; un cristal por cámara.
Pseudosamanea guachapele (Kunth) Harms.
Madera con duramen marrón. Olor y sabor no distintivo. Lustre mediano a alto. Grano entrecruzado. Textura mediana. Moderadamente dura y pesada a dura y pesada.
Anillos de crecimiento definidos por reducción del diámetro radial y engrosamiento de las paredes de las fibras, ocasionalmente por células parenquimáticas cristalíferas (X2676). Porosidad difusa. Poros sin patrón definido de disposición, solitarios y múltiples radiales de 2-3 (-6), ocasionalmente arracimados. Platinas de perforación simples. Punteaduras intervasculares alternas, circulares a ovaladas, ocasionalmente poligonales (X3711), pequeñas a medianas, ornadas. Punteaduras radiovasculares similares a las intervasculares. Depósitos de goma presentes. Fibras no septadas, paredes medianas a gruesas (delgadas en X3711), punteaduras indistintamente areoladas. Parénquima paratraqueal vasicéntrico ancho, aliforme de ala corta, confluente, ocasionalmente apotraqueal difuso y en islas dispersas, fusiforme (poco) y en series de 2-4 células. Radios homocelulares de células procumbentes. Cristales prismáticos en series parenquimáticas cristalíferas, largas y abundantes; un cristal por cámara, ocasionalmente dos (X3711).
Samanea saman (Jacq.) Merr. (Figura 6b).
Madera con albura de color amarillo y duramen marrón, transición abrupta entre albura y duramen. Olor y sabor no distintivo. Lustre mediano. Grano inclinado a entrecruzado. Textura mediana. Moderadamente dura y pesada a dura y pesada.
Anillos de crecimiento no definidos. Porosidad difusa. Poros sin patrón definido de disposición, solitarios y múltiples radiales de 2-4 (-6). Platinas de perforación simples. Punteaduras intervasculares alternas, circulares a ovaladas, medianas, ornadas. Punteaduras radiovasculares similares a las intervasculares. Depósitos de goma presentes. Fibras no septadas, paredes medianas a moderadamente gruesas, punteaduras indistintamente areoladas. Parénquima apotraqueal difuso, paratraqueal vasicéntrico ancho, aliforme de ala corta, confluente; en series de 2-4 (-6) células. Radios homocelulares de células procumbentes. Cristales prismáticos en series parenquimáticas cristalíferas, largas y abundantes; un cristal por cámara.
Stryphnodendron microstachyum Poepp.; S. polystachyum (Miq.) Kleinhoonte
Madera con albura amarilla y duramen marrón (S. polystachyum) a marrón rosáceo (S. microstachyum). Olor y sabor no distintivo. Lustre media-no. Grano recto a inclinado, hasta entrecruzado en S. polystachyum. Textura fina. Blanda y liviana a moderadamente dura y pesada.
Anillos de crecimiento no definidos a ligeramente definidos por reducción de diámetro radial de las fibras. Porosidad difusa. Poros sin patrón definido de disposición, solitarios y múltiples radiales de 2-3 (-4) en S. polystachyum, 2-5 en S. microstachyum, arracimados. Platinas de perforación simples. Punteaduras intervasculares alternas, circulares a ovaladas, medianas (S. microstachyum) o pequeñas a medianas (S. polystachyum), ornadas. Punteaduras radiovasculares similares a las intervasculares. Depósitos de goma presentes en los poros. Fibras no septadas, paredes delgadas a gruesas, punteaduras indistintamente areoladas. Parénquima apotraqueal difuso, paratraqueal vasicéntrico delgado y ancho, aliforme de ala corta; presencia de bandas con más de tres células de ancho y marginales en S. polystachyum (X1781); fusiforme (poco) y en series de 2-4 células. Radios homocelulares de células procumbentes. Cristales prismáticos en series parenquimáticas cristalíferas, largas y abundantes, predominantemente en el parénquima difuso; un cristal por cámara, ocasionalmente 2 (S. polystachyum).
Zygia longifolia (Humb. & Bonpl. ex Willd.) Brit-ton & Rose (Figura 6c).
Madera de color amarillo, sin transición entre albura y duramen. Olor y sabor no distintivo. Lustre mediano. Grano inclinado a entrecruzado. Textura moderadamente gruesa. Dura y pesada.
Anillos de crecimiento no definidos. Porosidad difusa. Poros sin patrón definido de disposición, solitarios y múltiples radiales de 2-3 (-5), ocasionalmente arracimados. Platinas de perforación simples. Punteaduras intervasculares alternas, circulares a ovaladas, diminutas a pequeñas, ornadas. Punteaduras radiovasculares similares a las intervasculares. Depósitos de goma presentes, abundantes. Fibras no septadas, paredes gruesas a muy gruesas, punteaduras indistintamente areoladas. Parénquima en bandas anchas abundantes, ocasionalmente vasicéntrico ancho y aliforme de ala corta; fusiforme (poco) y en series de 2-4 células. Radios homocelulares de células procumbentes. Cristales prismáticos en series parenquimáticas cristalíferas; un cristal por cámara.
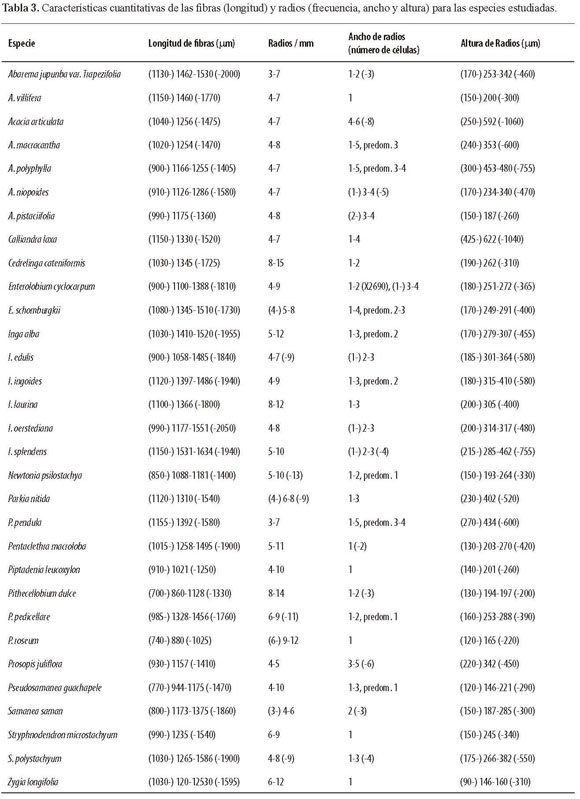
En las tablas 2 y 3 se presentan los resultados correspondientes a características cuantitativas de vasos, fibras y radios.

DISCUSIÓN
Las diferentes especies estudiadas muestran una estructura anatómica bastante uniforme entre sí en algunas características. La composición de los radios y las características de los cristales fueron las que mantuvieron mayor uniformidad y en todo el material se presentaron radios exclusivamente homocelulares de células procumbentes (Figuras 4b y 5c), mientras que los cristales fueron sólo de tipo prismático, presentándose en forma de series parenquimáticas cristalíferas, generalmente largas y abundantes. Con respecto al parénquima axial, aunque lo más común fue la presencia de parénquima paratraqueal vasicéntrico ancho combinado aliforme de ala corta y confluente (Figuras 1a, 1b, 1c, 5a, 6a y 6b), se observó la presencia de otros tipos de parénquima como apotraqueal (difuso en islas dispersas) (Figura 6b) bandas anchas (Figuras 3a y 6c) y ocasionalmente marginal (Figura 6a). En relación a los vasos se presentó una notable uniformidad entre las especies estudiadas y las principales variaciones se remiten a características dimensionales (diámetro de vasos, diámetro de punteaduras, frecuencia de vasos).
Apesar de la homogeneidad estructural, se observaron algunas características que permiten establecer grupos, siendo una de las más notables la presencia o ausencia de septas en las fibras: en el género Inga se presentó, de manera constante, el desarrollo de fibras septadas (Figuras 5b y 5c), al igual que en las especies Albizia niopoides y Enterolobium schomburgkii. Otra característica importante fue el ancho de los radios, el cual varió desde exclusiva o predominantemente uniseriado hasta radios de 5 células de ancho. Respecto al parénquima axial, lo común fue la presencia de parénquima paratraqueal vasicéntrico ancho combinado con aliforme y confluente. Sin embargo, en Calliandra laxa (Figura 3a) y Zygia longifolia (Figura 6c) se observó parénquima exclusivamente en bandas anchas, mientras que en Cedrelinga cateniformis (Figura 4a) se presentó parénquima predominantemente paratraqueal vasicéntrico delgado. Adicionalmente, en 11 especies se observó, en baja proporción, la presencia de parénquima apotraqueal, bien sea de forma difusa o como islas dispersas. El grosor de paredes de las fibras también mostró un amplio rango de variación, pudiendo encontrarse especies con fibras de paredes muy delgadas o delgadas (Figura 3b) hasta especies con fibras de paredes gruesas a muy gruesas (Figura 3a). Es notable indicar que dicha variación se observó entre especies de un mismo género, tal como fue el caso de Enterolobium. La variación existente en algunas carac terísticas permitió elaborar la siguiente clave de identificación:
1 a. Fibras septadas presentes ....................................................................................................................... 2
1 b. Fibras septadas ausentes ........................................................................................................................ 6
2 b. Punteaduras intervasculares diminutas ausentes .......................................................................................... 4
3 a. Fibras de paredes gruesas a muy gruesas, parénquima apotraqueal difuso presente ............................................ Enterolobium schomburgkii
3 b. Fibras de paredes medianas a gruesas, parénquima exclusivamente de tipo paratraqueal....................................... Albizia niopoides
4 a. Fibras septadas y no septadas................................................................................................................... Inga laurina
4 b. Fibras exclusivamente septadas ................................................................................................................ 5
5 a. Parénquima apotraqueal en islas dispersas presente ...................................................................................... Inga alba, I. ingoides, I. splendens
5 b. Parénquima apotraqueal en islas dispersas ausente ....................................................................................... I. edulis, I. oerstediana
6 a. Parénquima exclusiva o predominantemente en bandas anchas ........................................................................ 7
6 b. Parénquima en bandas anchas ausente o combinado con otro tipo.................................................................... 9
7 a. Radios exclusivamente uniseriados ............................................................................................................. Zygya longifolia
7 b. Radios predominantemente con más de una célula de ancho ........................................................................... 8
8 a. Parénquima fusiforme abundante ............................................................................................................... Prosopis juliflora
8 b. Parénquima fusiforme ausente .................................................................................................................. Calliandra laxa
9 a. Parénquima predominantemente vasicéntrico delgado, cristales ausentes ......................................................... Cedrelinga cateniformis
9 b. Parénquima predominantemente vasicéntrico ancho, aliforme, confluente; cristales presentes .............................. 10
10 a. Radios exclusiva o predominantemente uniseriados ..................................................................................... 11
10 b. Radios predominantemente con más de una célula de ancho ........................................................................ 18
11 a. Parénquima unilateral presente ............................................................................................................... 12
11 b. Parénquima unilateral ausente ................................................................................................................ 14
12 a. Parénquima en bandas anchas ausente .................................................................................................... Pithecellobium roseum
12 b. Parénquima en bandas anchas ausente .................................................................................................... 13
13 a. Poros pequeños (diámetro promedio < 100 µm.), parénquima marginal presente, radios exclusivamente uniseriados.................................................................................................................................................. Piptadenia leucoxylon
13 b. Poros medianos (diámetro promedio de 100-200 µm.), parénquima marginal ausente, radios de 1-2 células de ancho, predominantemente uniseriados ................................................................................................................................................. Newtonia psilostachya
14 a. Anillos de crecimiento no definidos, fibras exclusivamente de paredes delgadas ................................................ Abarema villifera
14 b. Anillos de crecimiento definidos a ligeramente definidos, fibras de paredes medianas y/o gruesas presentes ................................................................................................................................................... 15
15 a. Punteaduras intervasculares con diámetro de 8,75-10 µm ............................................................................ Stryphnodendron microstachyum
15 b. Punteaduras intervasculares con diámetro menor de 7,5 µm. ........................................................................ 16
16 a. Parénquima marginal presente ................................................................................................................. Pentaclethra macroloba
16 b. Parénquima marginal ausente .................................................................................................................. 17
17 a. Punteaduras intervasculares diminutas, parénquima apotraqueal ausente ........................................................ Pithecellobium pedicellare
17 b. Punteaduras intervasculares pequeñas a medianas, parénquima apotraqueal difuso y en islas dispersas presente .................................................................................................................................................... Pseudosamanea guachapele
18 a. Frecuencia de poros mayor o igual a 8 poros/mm2 ...................................................................................... 19
18 b. Frecuencia de poros menor o igual a 7 poros por mm2.................................................................................. 22
19 a. Radios hasta de 4 células de ancho, poros con diámetro promedio inferior a 100 µm........................................... Albizia pistaciifolia
19 b. Radios de 5 (-6) células de ancho presentes, poros con diámetro promedio superior a 100 µm. ........................... 20
20 a. Parénquima marginal presente ................................................................................................................ Acacia polyphylla
20 b. Parénquima marginal ausente .................................................................................................................21
21 a. Parénquima predominantemente en series de 4-7 células ............................................................................. Acacia articulata
21 b. Parénquima predominantemente en series de 2 células ................................................................................ Acacia macracantha
22 a. Punteaduras intervasculares diminutas a pequeñas ..................................................................................... Abarema jupunba var. trapezifolia
22 b. Punteaduras medianas presentes ............................................................................................................ 23
23 a. Parénquima apotraqueal presente ........................................................................................................... 24
23 b. Parénquima apotraqueal ausente ............................................................................................................ 27
24 a. Fibras con paredes muy delgadas ............................................................................................................ Parkia nitida
24 b. Fibras con paredes desde delgadas hasta gruesas ...................................................................................... 25
25 a. Parénquima fusiforme presente ............................................................................................................... 26
25 b. Parénquima fusiforme ausente ................................................................................................................ Samanea saman
26 a. Parénquima apotraqueal en islas dispersas presente ................................................................................... Pithecellobium dulce
26 b. Parénquima apotraqueal en islas dispersas ausente .................................................................................... Stryphnodendron polystachium
27 a. Anillos de crecimiento indistintos, radios de 1-2 células de ancho, parénquima en series de 2-4 células ...................................................................................................................................................... Enterolobium cyclocarpum
27 b. Anillos de crecimiento definidos, radios de 1-5 células de ancho, parénquima en series de (2-) 4-6 células ........................................................................................................................................................... Parkia pendula
Normalmente se considera que las diferentes subfamilias de las Leguminosae se caracterizan por poseer una estructura bastante homogénea y en el presente estudio se observaron ciertas características que confirman dicha homogeneidad, especialmente en lo relacionado con el tipo de parénquima axial, la composición de los radios, el tipo y la ubicación de cristales. Sin embargo, es difícil establecer una descripción precisa que abarque a los diferentes miembros de la subfamilia. Existen variaciones en características físicas como el color, tipo de transición entre albura y duramen, dirección de grano, textura y grados de peso, y dureza. Anatómicamente se presentan variaciones en cuanto a presencia o ausencia de anillos de crecimiento, diámetro de poros, tamaño de punteaduras, grosor de paredes de las fibras, presencia o ausencia de septas en las fibras, ancho y altura de radios. Adicionalmente, aunque es común la presencia de parénquima paratraqueal vasicéntrico ancho, aliforme de ala corta y confluente, se presentan casos en donde es predominantemente vasicéntrico delgado o bandas anchas, así como también se puede combinar apotraqueal difuso o en islas dispersas con los tres tipos anteriormente mencionados.
Con base en las características del material estudiado, se pueden diferenciar dos grupos: uno donde se incluyen las especies con fibras septadas y otro correspondiente a las especies con fibras no septadas. El primer grupo se encuentra representado por ocho especies (25.81% del total estudiado) pertenecientes a tres géneros: Albizia, Enterolobium e Inga. Todas las especies de Inga se caracterizaron por presentar fibras exclusivamente septadas, excepto I. laurina, donde se observó una combinación de fibras septadas y no septadas. En el caso de Albizia y Enterolobium, presentaron un comportamiento similar en el sentido de que incluyen especies con fibras septadas y especies con fibras exclusivamente no septadas. Baretta-Kuipers (1981) menciona que el género Albizia se caracteriza por presentar fibras septadas y es una de las características que utiliza para separarlo de Pithecellobium y Samanea.
Lo encontrado en el presente estudio indica que no siempre van a existir fibras septadas en Albizia, ya que las mismas fueron observadas sólo en A. niopoides y no se encontraron en A. pistaciifolia. Inside Wood (2008) confirma la combinación de fibras septadas y no septadas al presentar la descripción de 30 especies de este género y reportar la ausencia de fibras septadas en A. corymbosa, A. inundata y A. julibrissin. Chauhan & Dayal (1985) también confirman la presencia de especies con fibras exclusivamente septadas y especies con fibras exclusivamente no septadas, así como también algunas especies donde se combinan los dos tipos de fibras, basándose en una descripción realizada sobre diez especies del género Albizia en India. Con respecto al género Inga, las descripciones realizadas de diferentes especies (Corothie 1967, Baretta-Kuipers 1981, JUNAC 1981, Mainieri & Peres 1989, Espinoza & Melandri 2000, Miller & Détienne 2001) confirman que es un género donde es común la presencia de fibras septadas; sin embargo, Castro et al. (1992) indican que en I. stipularis no se presentan fibras septadas, reporte que no coincide con lo señalado por Evans et al. (2006), quienes mencionan la presencia de fibras septadas en esta especie. Es importante destacar que en la mayoría de las descripciones correspondientes a especies del género Inga se habla de fibras conspicuamente tabicadas o septadas, sin embargo en Inga laurina se presentó una combinación de fibras septadas y no septadas. Con relación al género Enterolobium, descripciones como las presentadas por Kribs (1968) y Mainieri & Peres (1989) confirman que se pueden presentar especies con fibras septadas y especies con fibras exclusivamente no septadas.
El parénquima axial también mostró amplias variaciones a pesar de ser común la presencia de parénquima paratraqueal vasicéntrico ancho, aliforme de ala corta y confluente. Sólo tres especies (9.68% del total estudiado) no presentaron los tipos de parénquima antes mencionados: Calliandra laxa, con parénquima exclusivamente en bandas anchas; Cedrelinga cateniformis, con parénquima predominantemente de tipo paratraqueal vasicéntrico delgado, y Zygia longifolia, donde el parénquima es de bandas anchas y ocasionalmente se observó el vasicéntrico ancho y aliforme de ala corta. En especies como Prosopis juliflora, aún cuando predomina el parénquima en bandas anchas, fue común encontrar parénquima aliforme de ala corta y confluente. Baretta Kuipers (1979) señala que la presencia de parénquima en bandas es una característica poco común en la Mimosoideae. La combinación de los tipos de parénquima mencionados con apotraqueal difuso y/o en islas dispersas se presentó en 13 especies (41.93% del total estudiado) pertenecientes a los géneros Abarema, Enterolobium, Inga, Parkia, Pentaclethra, Pithecellobium, Prosopis, Pseudosamanea, Samanea y Stryphnodendron. En comparación con las otras subfamilias de Leguminosae, es importante señalar que Espinoza de P. & Melandri (2006) indican que en 68 especies de Caesalpinoideae procedentes de Venezuela no se encontró parénquima apotraqueal, mientras que Espinoza de P. & León (2003) encontraron parénquima apotraqueal sólo en tres especies (5.36%) de las 56 estudiadas para la subfamilia Papilionoideae. En relación al parénquima radial, la característica que se mantuvo de manera más constante en todas las especies estudiadas fue el tipo de radio en cuanto a composición: el 100% del material estudiado se caracterizó por poseer radios exclusivamente homocelulares de células procumbentes, a diferencia de lo encontrado por Espinoza de P. & León (2003) para especies de la subfamilia Papilionoideae en Venezuela, donde un 38% de las especies estudiadas presentan radios heterocelulares, aún cuando en muchos casos predominen los homocelulares, mientras que para la subfamilia Caesalpinoideae cerca del 62% de las especies estudiadas en Venezuela presentan radios heterocelulares (Espinoza de P. & Melandri 2006). Gasson (1996) también reporta la presencia de radios heterocelulares en algunos géneros de la tribu Swartzieae de la subfamilia Papilionoideae. Respecto al ancho de los radios, se observó una amplia variación: se encontraron especies con radios exclusivamente uniseriados hasta especies con radios predominantemente de 4-5 células de ancho. Los radios exclusivamente uniseriados se presentaron en cinco especies (16.13%), mientras que cuatro especies (12.9%) presentaron radios que pueden llegar hasta tres células de ancho, pero con un notable predominio de los uniseriados. Cerca del 23% de las especies presentaron radios predominantemente con 3 o más células de ancho, siendo la especie Acacia articulata la que mostró mayor ancho de radios con 4-6 (-8) células de ancho. La altura de los radios mostró un comportamiento uniforme y sólo dos especies (Acacia articulata, Calliandra laxa) presentaron radios con alturas promedio superior a 500 µm.
A nivel de los elementos de conducción se observó una notable homogeneidad en cuanto a características cualitativas, pero considerables variaciones en características cuantitativas. La frecuencia de poros varió desde un mínimo de 1 poro/mm2 (Enterolobium cyclocarpum, Parkia pendula) hasta un máximo de 58 poros/mm2 (Piptadenia leucoxylon). De acuerdo a lo indicado por el IAWA Committee (1989), diez especies (32.25% del total) se ubican en la categoría I de frecuencia de poros (< 5 poros/mm2), once especies (35.49%) corresponden a la categoría II (5-20 poros/mm2), ocho especies (25.81%) tienen valores que las ubican en las categorías I y II, una especie (3.23%) presenta valores que la ubica en las categorías II y III (20-40 poros/ mm2) y una especie (3.23%) se ubica en la categoría IV (40-100 poros/mm2). En general, el 93.55% del material estudiado se incluye en las categorías II y III de frecuencia de poros establecida por el IAWA Committee (1989). En relación al diámetro tangencial de los poros, sólo cuatro especies (12.90%) presentaron valores promedio inferior a 100 µm (categoría II de IAWA Committee, 1989); los diámetros promedio superiores a 200 µm (categoría IV de IAWA Committee, 1989) se presentaron en 14 especies (45.16% del total), el mayor de ellos en Cedrelinga cateniformis con 400 µm. Es importante señalar que, según Baretta-Kuipers (1981), características como diámetro y frecuencia de poros no son importantes para la diferenciación dentro de las Leguminosae; sin embargo, el presente estudio indica que sí hay diferencias notables en algunas especies (Tabla 2), pudiendo ser utilizadas en la respectiva clave de identificación. Especies como Cedrelinga cateniformis muestran un diámetro de poros notablemente superior al resto de las especies estudiadas y, por tanto, desde el punto de vista taxonómico adquiere importancia dentro de la subfamilia Mimosoideae.
Otra característica que mostró un comportamiento bastante uniforme fue la relacionada con la presencia, ubicación y tipo de cristales: 30 de las especies estudiadas (96.77%) presentaron cristales prismáticos formando series parenquimáticas cristalíferas, generalmente largas y abundantes. Cedrelinga cateniformis fue la única especie donde no se observó ningún tipo de cristales y, aparentemente, presenta abundantes cámaras cristalíferas vacías. La ausencia de cristales en esta especie ha sido reportada por otros autores (Nardi & Edlmann 1992, Espinoza de P. & Melandri 2000). Un reporte inusual en cuanto a cristales es el presentado por Paula (2003) para Parkia multijuga, donde indica la presencia de cristales en células parenquimáticas radiales, observación que no coincide con lo encontrado en el presente estudio.
CONCLUSIONES
Las características que mantuvieron mayor homogeneidad entre las 31 especies estudiadas fueron la presencia de radios exclusivamente homocelulares de células procumbentes y los cristales prismáticos formando series en el parénquima axial. Todas las especies estudiadas mostraron el mismo tipo de radio y el 96.77% de las especies presentó el tipo de cristal antes mencionado, siendo Cedrelinga cateniformis la única especie donde no se encontró ningún tipo de cristal. Igualmente, los caracteres cualitativos de los vasos (porosidad, agrupación, disposición, contenido de los vasos, tipo de punteaduras intervasculares y radiovasculares y tipo de platina de perforación) mostraron uniformidad entre las diferentes especies estudiadas. El parénquima axial que se manifestó de manera más frecuente fue el paratraqueal vasicéntrico ancho, aliforme de ala corta y confluente. Sólo en Calliandra laxa, Cedrelinga cateniformis, Prosopis juliflora y Zygia longifolia se encontró el predominio de tipos de parénquima diferentes al antes mencionado.
Las fibras fueron uno de los elementos leñosos que mostraron mayor grado de variación, pudiéndose establecer dos grandes grupos: un grupo con presencia de fibras septadas y un segundo grupo que incluye especies con fibras exclusivamente septadas. También se observó variación con respecto al grosor de paredes de las fibras, encontrándose especies con fibras de paredes desde muy delgadas hasta especies con fibras de paredes muy gruesas.
Las características cuantitativas de los vasos (diámetro de poros y punteaduras, frecuencia de poros) también mostraron diferencias entre las especies estudiadas y se pueden considerar como un carácter de valor para la diferenciación de grupos de especies.Los radios de las especies estudiadas, a pesar de mantener uniformidad en cuanto a composición, muestran suficiente variación en cuanto a número de células de ancho como para poder establecer grupos dentro de la subfamilia. Se encontraron especies con radios desde exclusivamente uniseriados hasta especies con radios predominantemente con 3 o más células de ancho.
REFERENCIAS BIBLIOGRÁFICAS
APG. 2003. An Update of the Angiosperm Phylogeny Group Classification for the Orders and Families of Flowering Plants. APG II. Botanical Journal of the Linnean Society 141: 399-436.
Bank, H. & P. Gasson. 2000. Pollen Morphology and Wood Anatomy of the Crudia Group (Leguminosae, Caesalpinoideae, Detarieae). Botanical Journal of the Linnean Society 134: 19-59.
Barajas, J. & C. León. 1989. Anatomía de maderas de México: especies de una selva baja caducifolia. Universidad Nacional Autónoma de México. Instituto de Biología. Publicaciones especiales 16. México D.F. Pg. 126.
Barajas, M., G. Ángeles & P. Solís. 1997. Anatomía de maderas de México: especies de una selva alta perennifolia I. Universidad Nacional Autónoma de México. Instituto de Biología. Publicaciones especiales 16. México D.F. Pg. 126.
Baretta-Kuipers, T. 1979. Wood Anatomy of Archidendron F. v. Mueller, Mimosoideae, Leguminosae. IAWA Bulletin 2/3: 47-50.
Baretta-Kuipers, T. 1981. Wood Anatomy of Leguminosae: Its Relevance to Taxonomy. En: Pol-hill, R. & P. Raven (eds.). Advances in Legume Systematics: 677-705.
Castro, A., J. Alves & F. Vasconcellos. 1992. Ocorrencia de fibres lenhosas septadas em madeiras da Amazonia. Boletim do Museu Paraense Emilio Goeldi. Botánica 8: 191-201.
Chauhan, L. & R. Dayal. 1985. Wood Anatomy of the Indian Albizias. IAWA Bulletin 6: 213-218.
Corothie, H. 1967. Estructura anatómica de 47 maderas de la Guayana venezolana. Laboratorio Nacional de Productos Forestales. Universidad de Los Andes yMinisterio de Agricultura y Cría. Mérida, Venezuela.
Cronquist, A. 1981. An Integrated System of Classification of Flowering Plants. Columbia University Press. NewYork. Pg. 1262.
Cumbie, B. 1960. Anatomical Studies on the Leguminosae. Tropical Woods 113: 1-47.
Espinoza de P., N. & W. León H. 2003. Estudio anatómico del leño de 56 especies de la subfamilia Papilionoideae (Leguminosae) de Venezuela. Consejo de Desarrollo Científico, Humanístico y Tecnológico. Universidad de Los Andes. Mérida, Venezuela. Pg. 145.
Espinoza de P., N. & J. Melandri. 2000. Estudio anatómico del leño de cinco especies de la subfamilia Mimosoideae en Venezuela. Revista Pittieria 29/30: 75-88.
Espinoza de P., N. & J. Melandri. 2006. Anatomía de la madera de 68 especies de la subfamilia Caesalpinoideae (Leguminosae) en Venezuela. Consejo de Desarrollo Científico, Humanístico y Tecnológico. Universidad de Los Andes. Mérida, Venezuela. Pg. 189.
Evans, J. P.E. Gasson &G.P. Lewis. 2006. Wood Anatomy of the Mimosoideae (Leguminosae). IAWA Journal Supplement 5: Pg.117.
Gasson, P. 1996. Wood Anatomy of the Tribe Swartzieae with Comments on Related Papilionoid and Caesalpinioid Leguminosae. IAWA Journal 17: 45-75.
Gasson, P. 1999. Wood Anatomy of the Tribe Dipterygeae with Comments on Related Papilionoid and Caesalpinoid Leguminosae. IAWA Journal 20: 441-455.
Gasson, P. 2000. Does Wood Anatomy Support Tribal and Generic Classification in Papilionoideae- Leguminosae? En Herenden P.& A. Bruneau (eds.). Advances in Legume Systematics Part 9: 201-215.
Höhn, A. 1999. Wood Anatomy of Selected West African Species of Caesalpinoideae and Mimosoideae (Leguminosae): A Comparative Study. IAWA Journal 20: 115-146.
IAWA Committee. 1989. IAWA List of Microscopic Features for Hardwood Identification. IAWA Bulletin 10: 219-332.
Inside Wood. 2008. Disponible en: http://insidewood.lib.ncsu.edu/search, consultado en marzo de 2008.
JUNAC. 1981. Descripción general y anatómica de 105 maderas del grupo andino. Junta del Acuerdo de Cartagena. Lima.
Kribs, D. 1968. Commercial Foreign Woods in the American Market. Dover Publications New York.
Loureiro, A. & M. Da Silva. 1981. Estudo dendrológico e anatômico do lenho de 7 espécies e 3 subespécies de Dimorphandra (Leguminosae-Caesalpinoideae). Acta Amazonica 13: 149-170.
Loureiro, A., F. Vasconcellos & M. Da Silva. 1983. Contribuçao ao estudo anatômico do lenho de 5 espécies de Sclerolobium e 5 espécies de Tachigalia (Leguminosae) da Amazónia. Acta Amazonica 13: 149-170.
Mabberley, D. 1990. The Plant Book. Cambridge University Press. New York.
Mainieri, C. & J. Peres. 1989. Fichas de caracteristicas das madeiras brasileiras. Instituto de Pesquisas Tropicales. Sao Paulo.
Metcalfe, C. & L. Chalk. 1950. Anatomy of the Dicotyledons Vol. I. Oxford University Press. Oxford.
Miller, R. & P. Détienne. 2001. Major Timber Trees of Guyana. Wood Anatomy. Tropenbos International. Wageningen, Holanda.
Nardi, R. & M. Edlmann. 1992. Legnami tropicali importati in Italia: Anatomia e identificazione. Vol. II: America Latina. Istituto di Assestamento e Tecnología Forestale. Universita di Firenze. Florencia.
Paula, J. de 2003. Caracterizaçao anatômica da madeira de sete espécies da Amazônia con vistas a produção de energia e papel. Acta Amazonica 33: 243-266.
Record, S. &R. Hess. 1949. Timbers of the New World. 4th edición. Yale University Press. New Haven, Connecticut.
Licencia
Colombia Forestal conserva los derechos patrimoniales (copyright) de las obras publicadas, y favorece y permite la reutilización de las mismas bajo la licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional por lo cual se pueden copiar, usar, difundir, transmitir y exponer públicamente, siempre que:
Se reconozcan los créditos de la obra de la manera especificada por el autor o el licenciante (pero no de una manera que sugiera que tiene su apoyo o que apoyan el uso que hace de su obra).